
对于NH3不能用浓H2SO4干燥的原因分析正确的是
A.浓硫酸有强氧化性
B.NH3极易溶于水
C.NH3具有碱性物质的性质
D.两者会发生反应生成沉淀
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015湖南省怀化市小学课改高二上学期期末化学试卷(解析版) 题型:填空题
(每空2分,共16分)
I、恒温下,将a mol N2与b mol H2的混合气体通入一个固体容积的密闭容器中,发生如下反应:
N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)该反应的平衡常数表达式为:K=
(2)若反应进行到某时刻t时,nt(N2)=8 mol,nt(NH3)=4 mol,计算 a= 。当反应达到平衡时,混合气体的体积为537.6 L(标况下),其中NH3的含量(体积分数)为25%。原混合气体中, a:b= 。
Ⅱ、反应mA+nB pC+qD在某温度下达到平衡。
pC+qD在某温度下达到平衡。
①若A、B、C 、D都是气体,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时C的物质的量浓度变为原来的1.6倍,则m、n、p、q的关系是m+n p+q(填“<”或“>”或“=”) 。
②若A、B、C ,D都为气体,且m+ n = p+q,则将气体体积压缩后A的物质的量将 _________(填“减小”“增大”“不变”),平衡______移动。(填“正向”或“逆向”或“不”)
③若给体系升温,B的物质的量减少,则正反应为 ________反应(填“放热”或“吸热”)
④若在体系中增加A的量,平衡不发生移动,则A肯定不能为_____态。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广州市高一上学期期末化学试卷(解析版) 题型:选择题
下列反应能用CO32- + 2H+ = CO2 ↑ + H2O表示的是
A.Na2CO3 + H2SO4= Na2SO4+ CO2 ↑ + H2O
B.CaCO3 + 2HCl =CaCl2 + CO2 ↑+ H2O
C.KHCO3 + HCl = KCl + CO2 ↑ + H2O
D.BaCO3 + 2HNO3 =Ba(NO3 )2+ CO2 ↑ + H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市昌平区高一上学期期末考试化学试卷(解析版) 题型:填空题
(6分)现有含NaCl、Na2SO4、Na2CO3和NaHCO3的固体混合物。某同学为测定其中各组分的含量,取部分样品溶于水,并设计了如下实验流程(所加试剂均为过量,反应①~③均为复分解反应)。
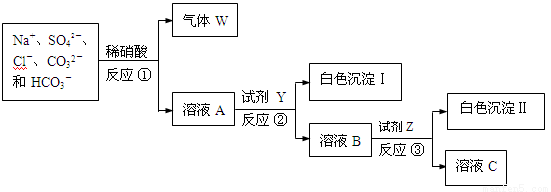
请回答:
 (1)气体W的化学式是 。
(1)气体W的化学式是 。
(2) 溶液A中主要存在的微粒除了Na+、SO42-、Cl-之外还有 。
溶液A中主要存在的微粒除了Na+、SO42-、Cl-之外还有 。
(3)反应②和③之后均需进行的操作的名称是 。
(4)试剂Y是 (填化学式)。
(5)测定各组分的含量,需要测的数据有:混合物总质量、白色沉淀Ⅰ和Ⅱ分别的质量和 。
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市昌平区高一上学期期末考试化学试卷(解析版) 题型:选择题
火法炼铜的原理为:Cu2S + O2 高温 2Cu + SO2,下列说法中,正确的是
A.Cu2S只作还原剂
B.该反应中的氧化剂只有O2
C.Cu2S 中的Cu元素被S元素还原
D.当1 mol O2参加反应时,共转移4 mol e-
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市昌平区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于Na2O和Na2O2 的说法中,正确的是
A.均能与水反应 B.氧元素的化合价均为-2
C.均为淡黄色固体 D.均能与CO2反应放出氧气
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市黄浦区高三上学期期末调研测试化学试卷(解析版) 题型:选择题
洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图。下列关于A的相关叙述正确的是

A.A在酸性条件下可以发生水解反应
B.1mol A和足量NaOH溶液反应,最多消耗9mol NaOH
C.A能和浓溴水发生加成和取代反应
D.A含4种官能团
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省眉山市高三第一次诊断性考试理综化学试卷(解析版) 题型:实验题
(14分)以铬铁矿(主要成分为FeO和Cr2O3 ,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(红矾钠的主要成分为重铬酸钠:Na2Cr2O7·2H2O),其主要工艺流程如下:
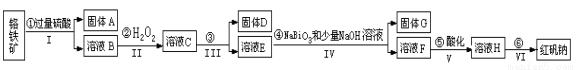
查阅资料得知:
i. 常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-。
ii.
物质 | 开始沉淀的pH值 | 完全沉淀的pH值 |
Fe(OH)3 | 2.7 | 3.7 |
Al(OH)3 | 3.4 | 4.4 |
Cr (OH)3 | 4.6 | 5.9 |
Fe(OH)2 | 7.5 | 9.7 |
Bi(OH)3 | 0.7 | 4.5 |
回答下列问题:
(1)反应之前先将矿石粉碎的目的是 。
(2)操作I、III、IV用到的主要玻璃仪器有玻璃棒和__________(填仪器名称)。
(3)写出④反应的离子反应方程式 。
(4)⑤中酸化是使CrO42-转化为Cr2O72-,写出该反应的离子方程式 。
(5)将溶液H经过下列操作,蒸发浓缩,__________,过滤,洗涤,干燥即得红矾钠。
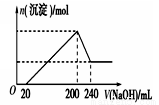
(6)取一定质量的固体D溶解于200mL的硫酸中,向所得溶液中加入5mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V关系如图所示,则硫酸的浓度为 ,固体D中含Fe化合物的物质的量为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com