
【题目】实验室用乙酸和正丁醇制备乙酸正丁酯,有关物质的相关数据如下:
化合物 | 密度/gcm-3 | 沸点/℃ | 溶解度/100g水 |
正丁醇 | 0.810 | 118.0 | 9 |
冰醋酸 | 1.049 | 118.1 | 互溶 |
乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
I.乙酸正丁酯粗产品的制备
在干燥的A中,装入沸石,加入11.5mL正丁醇和9.4mL冰酷酸,再加3~4滴浓硫酸,然后安装分水器(作用:实验过程中不断分离除去反应生成的水)。温度计及回流冷凝管,热冷凝回流反应。
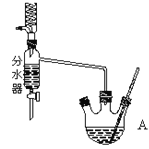
(1)实验过程中可能产生多种有机副产物。写出其中两种的结构简式:_________。
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是:_________。
II.乙酸正丁酯粗产品的制备
(3)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗,②蒸馏,③用无水MgSO4干燥,④用10%碳酸钠洗涤,正确的操作步骤是_________。
a ①②③④ b ③①④② c ①④①③② d ④①③②③
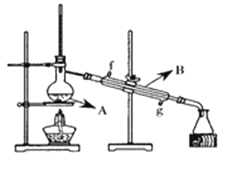
(4)将酯层采用下图所示装置蒸馏,图中仪器B的名称___________。冷却水从______口进入(填字母),蒸馏收集乙酸正丁酯产品时,应将温度控制在_________左右。
III.计算产率
(5)测量分水器内由乙酸与正丁醇反应生成的水体积为1.8mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率______。
【答案】CH3CH2CH2CH2OCH2CH2CH2CH3、CH2=CHCH2CH3 用分水器及时移走反应生成的水,减少生成物的浓度,使用过量醋酸,提高正丁醇的转化率 c 冷凝管 g 126.1℃ 79.4%
【解析】
I.(1)正丁醇在浓硫酸的作用下发生分子内或分子间的脱水反应等副反应,分别生成1丁烯或丁醚等,其结构简式为CH2=CHCH2CH3、CH3CH2CH2CH2OCH2CH2CH2CH3,故答案为:CH3CH2CH2CH2OCH2CH2CH2CH3、CH2=CHCH2CH3;
(2)实验中要提高乙酸正丁酯的产率,即使酯化反应平衡向右移动,采取的措施可以是是增大另一种反应物乙酸的浓度(用量)、减小生成物的浓度,通过乙酸乙酯的制取可以知道,由于乙酸乙酯的沸点低于水,我们采取将乙酸乙酯蒸出的措施,但本题中乙酸正丁酯的沸点比水的高,因此采用分水器及时移走反应生成的水的措施,故答案为:用分水器及时移走反应生成的水,减少生成物的浓度,使用过量醋酸,提高正丁醇的转化率;
Ⅱ.(3)乙酸正丁酯粗产品中含有的杂质:乙酸、正丁醇、水、丁醚等,分析题目给出的四种操作:①水洗②蒸馏③用无水MgSO4干燥④用10%碳酸钠溶液洗涤,结合操作的难易、顺序和必要性,如干燥要放在水洗或10%碳酸钠洗涤之后,蒸馏操作复杂,一般放在最后,可知正确的操作步骤是①④①③②,即C选项正确,故答案为:c;
(4)图中仪器B的作用为冷却蒸馏得到的馏分,名称是直形冷凝管,冷凝管的冷却水应“下进上出”,由题干的表格信息可知,乙酸正丁酯的沸点为126.1℃,因此蒸馏收集乙酸正丁酯产品时,应将温度控制在126.1℃,故答案为:(直形)冷凝管;g;126.1℃;
Ⅲ.根据反应的化学方程式可知,水的产率就是乙酸正丁酯的产率,根据公式![]() 可得,11.5mL正丁醇的质量为
可得,11.5mL正丁醇的质量为![]() ,物质的量为
,物质的量为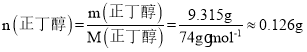 ,则完全反应生成水的物质的量为0.126mol,质量为0.126mol×18g/mol=2.268g,而实际生成水1.8g,则
,则完全反应生成水的物质的量为0.126mol,质量为0.126mol×18g/mol=2.268g,而实际生成水1.8g,则![]() ,故答案为:79.4%。
,故答案为:79.4%。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. NaHCO3(s) ![]() Na2CO3(s)
Na2CO3(s) ![]() NaOH(aq)
NaOH(aq)
B. Al(s)![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3(s)
Al(OH)3(s)
C. AgNO3(aq)![]() [Ag(NH3)2]+(aq)
[Ag(NH3)2]+(aq)![]() Ag(s)
Ag(s)
D. Fe2O3(s)![]() Fe(s)
Fe(s)![]() FeCl3(aq)
FeCl3(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用铁铆钉固定两个铜质零件的示意图,若该零件置于潮湿空气中,下列说法正确的是
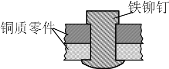
A.发生电化学腐蚀,铜为负极,铜极产生H2
B.铜易被腐蚀,铜极上发生还原反应,吸收O2
C.铁易被腐蚀,铁发生氧化反应,Fe-2e-=Fe2+
D.发生化学腐蚀:Fe + Cu2+ = Cu + Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素,它们在周期表中位置如图所示,下列说法正确的是![]()
![]()
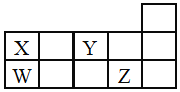
A.四种元素中原子半径最大为W,Y元素通常没有最高正价
B.酸性:![]()
C.![]() 、
、![]() 中所含化学键类型相同,熔点都很高
中所含化学键类型相同,熔点都很高
D.W、X形成的单质都是重要的半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M由两种元素组成,某研究小组按如图流程探究其组成:
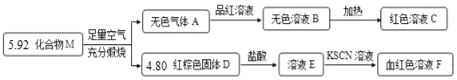
请回答:
(1)在制作印刷电路板的过程中常利用铜与溶液E的反应,反应的化学方程式为_____。
(2)将气体A通入溶液E中,溶液由黄色变成浅绿色,且酸性明显增强.写出该反应的离子方程式_____。
(3)化合物M的化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是![]()
![]()
A.1mol的碳烯![]() :
:![]() 含电子数为6
含电子数为6![]()
B.一定温度下,15g甲醛和乙酸的混合物含O原子数为![]()
![]()
C.常温常压下,![]() g乙醇中含有
g乙醇中含有![]() 键的个数为
键的个数为![]()
![]()
D.标准状况下,![]() L庚烷完全燃烧后生成的
L庚烷完全燃烧后生成的![]() 分子数为
分子数为![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下列氧化还原反应:
Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O。
(1)该反应的还原剂是________,还原产物是________。
(2)该反应中氧化剂与氧化产物的物质的量之比是________。
(3)当有2 mol HNO3参加反应时,被氧化的物质是________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠是一种应用广泛的金属,钠及其化合物在生产生活中应用广泛。某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图所示。
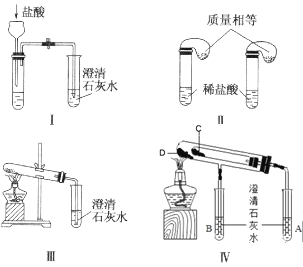
(1)只根据图中装置Ⅰ、Ⅱ所示实验,能够达到实验目的的是__(填装置序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式__、__;Ⅳ中现象为___;与实验Ⅲ相比,实验Ⅳ的优点___。
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管C中装入的固体是__(填化学式)。
(4)将适量钠投入下列溶液中,既能产生大量气体又能生成沉淀的是__(填写字母)
A.稀硫酸 B.氯化钠溶液 C.氯化镁溶液 D.硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组拟合成染料X和医药中间体Y。
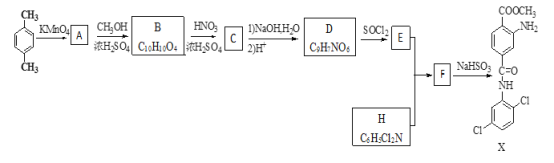
已知:①![]() ②
②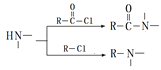 ③
③![]() ④
④![]() 。
。
(1)下列说法正确的是_________。
A.化合物A能与能与NaHCO3反应产生气体 B.X的分子式是C15H14Cl2O3N2
C.化合物C能发生取代、还原、加成反应 D.A→B,B→C的反应类型均为取代反应
(2)化合物D的结构简式是_________。
(3)写出E+H→F 的化学反应方程式__________________。
(4)写出化合物B(C10H10O4)同时符合下列条件的两种同分异构体的结构简式______________。
①与NaHCO3溶液反应,0.1mol该同分异构体能产生4.48L(标准状况下)CO2气体;②苯环上的一氯代物只有两种且苯环上的取代基不超过三个;③核磁共振氢谱有五种不同化学环境的氢,且峰面积比为1:2:2:2:3。
(5)设计以乙烯为原料合成制备Y(![]() )的合成路线________________(用流程图表示,无机试剂任选)。
)的合成路线________________(用流程图表示,无机试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com