
| Mg |
| 无水乙醚 |

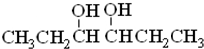 ,C为HOCH2CH2OH,故反应①可以是乙烯与溴发生加成反应生成B为BrCH2CH2Br,B发生水解反应生成C,由I分子与G分子相差1个水分子,应是G发生消去反应脱去1分子水生成I,故I为CH3CH2CH(OH)CH=CHCH3等,2分子G脱去2分子水形成六元环醚J,据此解答.
,C为HOCH2CH2OH,故反应①可以是乙烯与溴发生加成反应生成B为BrCH2CH2Br,B发生水解反应生成C,由I分子与G分子相差1个水分子,应是G发生消去反应脱去1分子水生成I,故I为CH3CH2CH(OH)CH=CHCH3等,2分子G脱去2分子水形成六元环醚J,据此解答.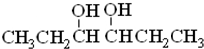 ,C为HOCH2CH2OH,故反应①可以是乙烯与溴发生加成反应生成B为BrCH2CH2Br,B发生水解反应生成C,由I分子与G分子相差1个水分子,应是G发生消去反应脱去1分子水生成I,故I为CH3CH2CH(OH)CH=CHCH3等,2分子G脱去2分子水形成六元环醚J,
,C为HOCH2CH2OH,故反应①可以是乙烯与溴发生加成反应生成B为BrCH2CH2Br,B发生水解反应生成C,由I分子与G分子相差1个水分子,应是G发生消去反应脱去1分子水生成I,故I为CH3CH2CH(OH)CH=CHCH3等,2分子G脱去2分子水形成六元环醚J,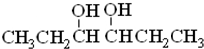 ,故答案为:乙二醇;
,故答案为:乙二醇;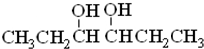 ;
;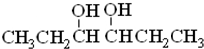 ,G发生消去反应生成I,六者均存在甲基的四面体结构,所有原子不可能处于同一平面,D为OHC-CHO,存在-CHO为平面结构,2个平面通过旋转碳碳单键可以处于同一平面,所有原子可能处于同一平面;
,G发生消去反应生成I,六者均存在甲基的四面体结构,所有原子不可能处于同一平面,D为OHC-CHO,存在-CHO为平面结构,2个平面通过旋转碳碳单键可以处于同一平面,所有原子可能处于同一平面;| 催化剂 |
| △ |
| 催化剂 |
| △ |
| 2×9+2-10 |
| 2 |
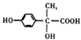 ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转 |
| B、能量低的电子只能在s轨道上运动,能量高的电子总是在f轨道上运动 |
| C、能层序数越大,s原子轨道的半径越大 |
| D、某微粒的最外层电子排布为2s22p6,则该微粒为Ne |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com