
ij��ȤС��ͬѧ���о�SO2��������ʡ�
(1)�Ƚ��±��е��������ʹ�ϵ����2��������X�Ļ�ѧʽ��  ��
��
��1�� | ��2�� |
C��CO��CO2��H2CO3��Na2CO3����NaHCO3�� | S ��SO2��SO3��X��Na2SO4��NaHSO4 |
(2)������ͼװ��������SO2������
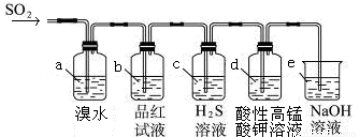
��װ ��a�е������ǣ� �� (��ܡ����ܡ�)˵��SO2��Ư����
��a�е������ǣ� �� (��ܡ����ܡ�)˵��SO2��Ư����
����װ��e����40 mL 2��5 mol•L��1 NaOH��Һ����Ӧ������4 ��8 g����
��8 g���� װ��IV�з�����Ӧ���ܻ�ѧ����ʽ�� ��
װ��IV�з�����Ӧ���ܻ�ѧ����ʽ�� ��
(3)��С��ļס�����λͬѧ������ͼװ�ü���̽��SO2������Ư���ԣ�
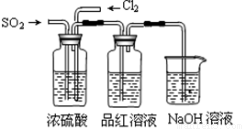
ͨ��һ��ʱ���ͬѧʵ�������Ʒ����Һ���� ����ɫ������ͬѧ��ʵ��������Ʒ����Һ��ʱ������Ʊ��Խ��Խdz���Ը��ݸ�ʵ��װ�ú�����ͬѧ��ʵ�����ش����⡣
����ɫ������ͬѧ��ʵ��������Ʒ����Һ��ʱ������Ʊ��Խ��Խdz���Ը��ݸ�ʵ��װ�ú�����ͬѧ��ʵ�����ش����⡣
���Է�����ͬѧʵ������У������ӷ���ʽ��ʾƷ����Һ����ɫ��ԭ���ǣ� ��
������Ϊ��ͬѧ������������Ʒ����Һ���Խ��Խdz�ģ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ����10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й�ҵ��������Ҫ��Ӧ�У��漰�û���Ӧ���ǣ� ��
A.�����ֹ� B.��ˮ��þ C.���ұ���� D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ɹŸ������¿�����ѧ���������棩 ���ͣ�ѡ����
ֻ��һ���Լ���������Na2SO4��AlCl3��NH4Cl��MgSO4������Һ�������Լ��ǣ� ��
A��HCl B��BaCl2  C��AgNO3 D��NaOH
C��AgNO3 D��NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ɹų���������ظ�����ͳһ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���0��1000 mol/L NaOH��Һ�ֱ�ζ�20.00 mL 0.1000 mol/L�����20.00 mL 0.1000 mol/L������Һ���õ�2���ζ����ߣ�����ͼ��ʾ��
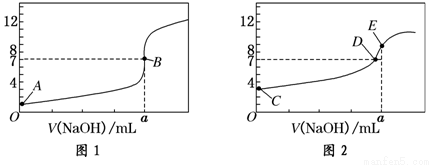
��HA��ʾ�ᣬ����˵����ȷ���ǣ� ��
A���ζ������������ͼ2
B���ﵽB��D״̬ʱ������Һ������Ũ�Ⱦ�Ϊc��Na+��=c��A����
C���ﵽB��E״̬ʱ����Ӧ���ĵ�n�� CH3COOH��>n��HCl��
D����0mL< V��NaOH��<20.00mLʱ����Ӧ�����Һ�и�����Ũ���ɴ�С��˳���Ϊc��A-��>c��N a+��>c��H+��>c��OH-��
a+��>c��H+��>c��OH-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ɹų���������ظ�����ͳһ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
N2(g)��H2(g)�����������澭�����¹�������NH3(g)������˵����ȷ�� ��
��
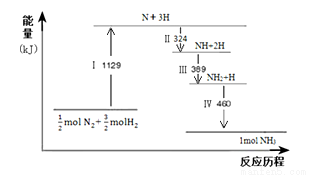
A�������ƻ��ľ�Ϊ���Լ�
B������NH2��H2����NH3
C������Ϊ���ȹ���
D��N2(g)+3H2(g) 2NH3(g) ��H��0
2NH3(g) ��H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ʮ��У����������������ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����( )
A�������£���ӦC(s)��CO2(g)=2CO(g)�����Է����У���÷�Ӧ�Ħ�H > 0
B����֪2CO(g)��O2(g)��2CO2(g) ��H����566 kJ��mol��1����CO��ȼ���Ȧ�H����283 kJ
C����֪H��(aq)��OH��(aq)=H2O(l) ��H����57.3 kJ��mol-1����ϡH2SO4��Һ��ϡBa(OH)2 ��Һ��Ӧ�ķ�Ӧ�Ȧ�H ==2��(��57.3) kJ��mol-1
D��500�桢30MPa�£���0.5mol N2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3kJ���Ȼ�ѧ����ʽΪ��N2(g)+3H2(g)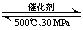 2NH3(g) ��H=��38.6 kJ��mol-1
2NH3(g) ��H=��38.6 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ʮ��У����������������ѧ�Ծ��������棩 ���ͣ�ѡ����
����װ�û�����ܴﵽʵ��Ŀ�ĵ���( )

A����ͼ1ʵ���֤���ǽ�����Cl��C��Si
B����ͼ2��ʾװ�ÿɳ�ȥNO2�е�NO
C����ͼ3װ���Ʊ�Fe(OH)2���ܽϳ�ʱ��۲�����ɫ
D��ͼ4ʵ��װ�ÿ�˵��ŨH2SO4������ˮ�ԡ�ǿ�����ԣ�SO2����Ư���ԡ���ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������ʡ��УЭ���������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
Ԫ��X�ĵ��ʼ�X��Y�γɵĻ������ܰ���ͼ��ʾ�Ĺ�ϵ����ת��������m��n,�Ҿ�Ϊ��������������˵����ȷ����
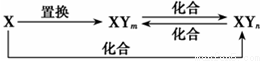
A. XΪFe��Y��ΪCl��Br
B. XΪFe��Yֻ��ΪCl
C. Xһ��Ϊ����Ԫ��
D. XΪFe��Y��ΪCl��Br��I
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������и����������������ѧ���������棩 ���ͣ�ѡ����
���и��������ڸ��������²��ܴ���������ǣ� ��
����pH=1����Һ��:NH4+��K+��ClO-��Cl-
����SO42-���ڵ���Һ��:Na+��Mg2+��Ca2+��I-
����NO3-���ڵ�ǿ������Һ��:NH4+��Ba2+��Fe2+��Br-
����c(H+)=1.0��10-1mol-L-1����Һ��:Na+��S2-��AlO2-��SO32-
�ݺ��д���Al3+����Һ:Na+��NH4+��SO42-��HCO3-
���д���Fe3+����Һ:Na+��Mg2+��NO3-��SCN-.
A.�� B.�٢ڢ� C.�ڢܢݢ� D.ȫ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com