
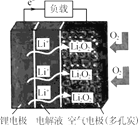
【题目】某新型锂空气二次电池放电情况如图所示,关于该电池的叙述正确的是
A.电解液应选择可传递Li+的水溶液
B.充电时,应将锂电极与电源正极相连
C.放电时,空气电极上发生的电极反应为 2Li++O2+2e-=Li2O2
D.充电时,若电路中转移0.5mol电子,空气电极的质量将减少3.5g
【答案】C
【解析】
在锂空气电池中,锂作负极,电极反应式为Li-e-=Li+,以空气中的氧气作为正极反应物,正极上是氧气得电子的还原反应,反应为2Li++O2+2e-=Li2O2,据此解答。
A.Li易与水反应,所以电解液不能选择可传递Li+的水溶液,A错误;
B.充电时,电池的负极连接电源的负极,所以应将锂电极与电源负极相连,B错误;
C.放电时,空气中的氧气作为正极反应物,正极上是氧气得电子的还原反应,反应为2Li++O2+2e-=Li2O2,C正确;
D.充电时,空气电极反应为Li2O2-2e-=2Li++O2,可见每转移2mol电子,空气电极的质量减少46g,若电路中转移0.5 mol电子,空气电极的质量将减少46g÷4=11.5g,D错误;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是
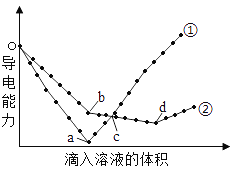
A.b→d反应的离子方程式为:H++OH-=H2O
B.o→a反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O
C.c点导电能力相同,所以两溶液中含有相同量的OH–
D.a、b两点Ba2+均沉淀完全,所以对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下述装置制取氯气,并用氯气进行下列实验。看图回答下列问题:

(1)A、B两仪器的名称:A________,B________。
(2)洗气装置C是为了除去Cl2中的HCl气体,D是为了干燥Cl2,则C、D中应分别放入下列溶液中的C______________;D______________。
①NaOH溶液 ②饱和食盐水 ③AgNO3溶液 ④浓H2SO4
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是______________________________。
(4)G是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成____________。反应的离子方程式是______________________,H是浸有NaBr溶液的棉花球,H处现象是棉花球表面变成________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2010年温哥华冬季奥运会上,有个别运动员因服用兴奋剂被取消参赛的资格。下图是检测出兴奋剂的某种同系物X的结构,关于X的说法正确的是( )
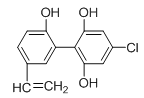
A. X分子中不可能所有原子都在同一平面上
B. X 遇到FeCl3溶液时显紫色,而且能使溴的四氯化碳溶液褪色
C. 1 mol X 与足量的浓溴水反应,最多消耗5 mol Br2
D. 1 mol X在一定条件下与足量的氢气反应,最多消耗1 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
Ⅰ(1)萘的结构式为![]() ,它的二氯代物有______种。
,它的二氯代物有______种。
(2)立方烷![]() 的六氯代物有______种。
的六氯代物有______种。
Ⅱ根据下列有机化合物的官能团,写出下列反应的方程式。

(1)A 发生银镜反应___________________________________________________________
(2) B与足量的碳酸钠溶液反应_____________________________________
(3)C在足量的氢氧化钠水溶液中反应__________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:


实验步骤: 在A中加入4.4 g异戊醇(![]() ),6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
),6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
(1)仪器B的名称是_________________。
(2)如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是________ (填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)在洗涤操作中,第一次水洗的主要目的是________,第二次水洗的主要目的是___________。
(4)分液漏斗在使用前须清洗干净并_______,在洗涤、分液操作中,应充分振荡,然后静置,待分层后_________________(填标号),
a.直接将乙酸异戊酯从分液漏斗上口倒出
b.直接将乙酸异戊酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(5)本实验中加入过量乙酸的目的是_________________。
(6)实验中加入少量无水MgSO4的目的是_____________。
(7)在蒸馏操作中,仪器选择及安装都正确的是_____________ (填标号) 。
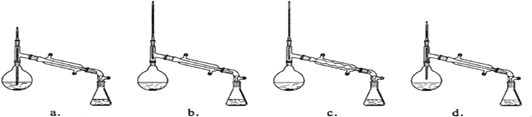
(8)本实验的产率是_____________
a. 30% b. 40% c. 50% d. 60%
(9)在进行蒸馏操作时,若从130 ℃开始收集馏分,会使实验的产率偏_____________ (填“高”或“低”),其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相容性方面有很好的应用前景。 PPG的一种合成路线如下:

已知:①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢;
②化合物B为单氯代烃:化合物C的分子式为C5H8;
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
④ 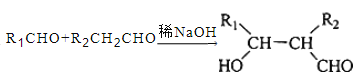 。
。
回答下列问题:
(1)A的结构简式为______________。
(2)由B生成C的化学方程式为________________________________________。
(3)由E和F生成G的反应类型为__________,G的化学名称为_____________。
(4)由D和H生成PPG的化学方程式为 ___________________________________。
(5)D的同分异构体中能同时满足下列条件的共有____种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体 ②既能发生银镜反应,又能发生皂化反应,其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是_________写结构简式):D的所有同分异构体在下列—种表征仪器中显示的信号(或数据)完全相同,该仪器是___________(填标号)。a.质谱仪 b.红外光谱仪c.元素分析仪d.核磁共振仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数小于36的X、Y、Z、R、W五种元素,其中X是周期表中原子半径最小的元素,Y是形成化合物种类最多的元素,Z原子基态时2p原子轨道上有3个未成对的电子,R单质占空气体积的![]() ;W的原子序数为29。回答下列问题:
;W的原子序数为29。回答下列问题:
(1)Y2X4分子中Y原子轨道的杂化类型为________,1mol Z2X4含有σ键的数目为 ________。
(2)化合物ZX3与化合物X2R的VSEPR构型相同,但立体构型不同,ZX3的立体构型为 ________,两种化合物分子中化学键的键角较小的是________(用分子式表示,下同)。
(3)与R同主族的三种非金属元素与X可形成结构相似的三种物质,试推测三者的稳定性由大到小的顺序________,理由是 ________;三者的沸点由高到低的顺序是 ________,解释原因________。
(4)元素Y的一种氧化物与元素Z的单质互为等电子体,元素Y的这种氧化物的分子式是________。
(5)W元素有________个运动状态不同的电子,其基态原子的价电子排布式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某学校实验室从化学试剂商店买同的硫酸试剂标签上的部分内容。据此下列说法正确的是
硫酸化学纯(CP)
(500mL)
品名:硫酸
化学式:H2SO4
相对分子质量:98
密度:1.84g / cm3
质量分数:98%
A.该硫酸的物质的量浓度为1.84mol/L
B.1mol Zn与足量的该硫酸反应产生2gH2
C.配制200mL 4.6mol/L的稀硫酸需取该硫酸50mL
D.该硫酸与等体积的水混合所得溶液的物质的量浓度等于9.2mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com