
����Ŀ������Aֻ����������һ��ȡ����B��C��D��C�Ľṹ��ʽ����ͼ��  ��B��D�ֱ���ǿ��Ĵ���Һ���ȣ���ֻ�ܵõ��л�������E�����Ϸ�Ӧ��B�Ľ�һ����Ӧ������ʾ��
��B��D�ֱ���ǿ��Ĵ���Һ���ȣ���ֻ�ܵõ��л�������E�����Ϸ�Ӧ��B�Ľ�һ����Ӧ������ʾ��
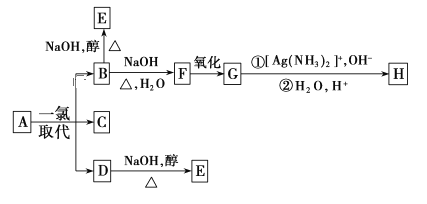
��ش��������⣺
(1)A�Ľṹ��ʽ��_________��
(2)H�Ľṹ��ʽ��________��
(3)Bת��ΪF�ķ�Ӧ����____��Ӧ(�Ӧ��������)��
(4)Bת��ΪE�ķ�Ӧ����_____��Ӧ(�Ӧ��������)��
(5)д���������ʼ�ת���Ļ�ѧ����ʽ��B��F��________����F��G��_______��
���𰸡�(CH3)3CCH2CH3 (CH3)3CCH2COOH )ȡ��(ˮ��) ��ȥ (CH3)3CCH2CH2Cl��H2O![]() (CH3)3CCH2CH2OH��HCl 2(CH3)3CCH2CH2OH��O2
(CH3)3CCH2CH2OH��HCl 2(CH3)3CCH2CH2OH��O2![]() 2(CH3)3CCH2CHO��2H2O
2(CH3)3CCH2CHO��2H2O
��������
����Aֻ����������һ��ȡ����B��C��D��C�Ľṹ��ʽ��![]() ����AΪ(CH3)3CCH2CH3��B��D�ֱ���ǿ��Ĵ���Һ���ȣ���ֻ�ܵõ��л�������E����EΪ(CH3)3CCH=CH2��B����ˮ�ⷴӦ����F��F������������������Ӧ����BΪ(CH3)3CCH2CH2Cl��DΪ(CH3)3CCH(Cl)CH3����FΪ(CH3)3CCH2CH2OH��GΪ(CH3)3CCH2CHO��HΪ(CH3)3CCH2COOH���ݴ˽��
����AΪ(CH3)3CCH2CH3��B��D�ֱ���ǿ��Ĵ���Һ���ȣ���ֻ�ܵõ��л�������E����EΪ(CH3)3CCH=CH2��B����ˮ�ⷴӦ����F��F������������������Ӧ����BΪ(CH3)3CCH2CH2Cl��DΪ(CH3)3CCH(Cl)CH3����FΪ(CH3)3CCH2CH2OH��GΪ(CH3)3CCH2CHO��HΪ(CH3)3CCH2COOH���ݴ˽��
����Aֻ����������һ��ȡ����B��C��D��C�Ľṹ��ʽ��![]() ����AΪ(CH3)3CCH2CH3��B��D�ֱ���ǿ��Ĵ���Һ���ȣ���ֻ�ܵõ��л�������E����EΪ(CH3)3CCH=CH2��B����ˮ�ⷴӦ����F��F������������������Ӧ����BΪ(CH3)3CCH2CH2Cl��DΪ(CH3)3CCH(Cl)CH3����FΪ(CH3)3CCH2CH2OH��GΪ(CH3)3CCH2CHO��HΪ(CH3)3CCH2COOH��
����AΪ(CH3)3CCH2CH3��B��D�ֱ���ǿ��Ĵ���Һ���ȣ���ֻ�ܵõ��л�������E����EΪ(CH3)3CCH=CH2��B����ˮ�ⷴӦ����F��F������������������Ӧ����BΪ(CH3)3CCH2CH2Cl��DΪ(CH3)3CCH(Cl)CH3����FΪ(CH3)3CCH2CH2OH��GΪ(CH3)3CCH2CHO��HΪ(CH3)3CCH2COOH��
(1)ͨ�����Ϸ���֪��A�ṹ��ʽΪ (CH3)3CCH2CH3��
(2)������������֪��H�Ľṹ��ʽ��(CH3)3CCH2COOH��
(3)Bת��ΪF��±����������ˮ�ⷴӦ��Ҳ����ȡ����Ӧ��
(4)Bת��ΪE��±������������ȥ��Ӧ��
(5)��B��F�Ļ�ѧ��Ӧ����ʽΪ��(CH3)3CCH2CH2Cl��H2O![]() (CH3)3CCH2CH2OH��HCl��
(CH3)3CCH2CH2OH��HCl��
��F��G�Ļ�ѧ��Ӧ����ʽΪ��2(CH3)3CCH2CH2OH��O2![]() 2(CH3)3CCH2CHO��2H2O��
2(CH3)3CCH2CHO��2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й��Ŵ������м����˴����Ŵ���ѧ���о��ɹ��������ݸ�Ŀ���м��أ���(��ҩ)������(KNO3)����ǡ�ɼľ̿���ϣ���Ϊ����糧���ҩ��������Ӧԭ��Ϊ��S+2KNO3+3C===K2S+N2��+3CO2����
(1)��ԭ�ӵļ۲�����Ų�ͼΪ___________���̻�ȼ�Ź����У���Ԫ���еĵ���ԾǨ�ķ�ʽ��___________��K��S��N��O����Ԫ�ص�һ�������ɴ�С��˳��Ϊ___________��������Ӧ�漰��Ԫ���е縺��������___________(��Ԫ�ط���)��
(2)̼Ԫ�س����γɳ�����������CO��CO2�⣬�����γ�C2O3(�ṹʽΪ![]() )��C2O3��ˮ��Ӧ�����ɲ���(HOOC��COOH)��
)��C2O3��ˮ��Ӧ�����ɲ���(HOOC��COOH)��
��C2O3��̼ԭ�ӵ��ӻ��������Ϊ___________��CO2���ӵ����幹��Ϊ___________��
�ڲ�����������(CH3CH2CH2COOH)����Է����������2�����ߵ��۵�ֱ�Ϊ101�桢-7.9�棬�������ֲ��������Ҫԭ�������______________________��
��CO����������������������Ϊ___________��
(3)�������صľ����ṹͼ���£�

����K+�Ⱦ����������K+����Ϊ___________������������Ϊdpm����ó���������ܶ�Ϊ___________g��cm��3(�ú�d��NA�Ĵ���ʽ��ʾ����NA��ʾ�����ӵ�������ֵ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ������CO2��H2��Ӧ���ɼ״���Ҳ�Ǽ���CO2��һ�ַ��������ݻ�Ϊ 1L �ĺ����ܱ������г���1mol CO2��3mol H2��һ�������·�����Ӧ�� CO2(g)��3H2(g)CH3OH(g)��H2O(g)��H����49.0 kJ/mol�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��
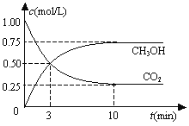
(1)�ﵽƽ���ʱ����_________min(����3������10��)����ǰ10min�ڣ���CO2Ũ�ȵı仯��ʾ�ķ�Ӧ������(CO2)��_________mol/(L�� min)��
(2)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������_________��
a.������ѹǿ���� b.���������c(CO2)���� c.��(CH3OH)����(H2O) d.c(CH3OH)��c(H2O)
(3)��ƽ���H2��ת������_________��ƽ�ⳣ�� K ��_________(����������һλС��)��Ϊ�����H2��ת���ʣ��ɲ�ȡ_________(����������������С��)CO2Ũ�ȵĴ�ʩ��
(4)��ҵ��Ҳ���� CO ��H2�ϳɼ״�
��֪����CO(g) + ![]() O2(g) = CO2(g) ��H1��-283.0 kJ/mol
O2(g) = CO2(g) ��H1��-283.0 kJ/mol
��H2(g) + ![]() O2(g) = H2O(g) ��H2��-241.8 kJ/mol
O2(g) = H2O(g) ��H2��-241.8 kJ/mol
��CH3OH(g) + ![]() O2(g) = CO2(g)+2H2O(g) ��H3��-673kJ/mol
O2(g) = CO2(g)+2H2O(g) ��H3��-673kJ/mol
��ӦCO(g) + 2H2(g) = CH3OH(g)��H��_________kJ/mol
(5)��ͼ�Ǽ״�ȼ�ϵ��ԭ��ʾ��ͼ����������ĵ缫��ӦʽΪ��_________��
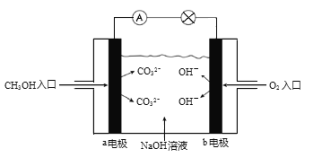
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��̬��A�IJ�����һ������ʯ�ͻ���ˮƽ����Ҫ��־���л���A��E�ܷ�����ͼ��ʾһϵ�б仯��������˵����ȷ����( )
![]()
A.A��B�ķ�Ӧ����Ϊ�ӳɷ�Ӧ
B.�������л���C��һ���д̼�����ζ������
C.����ʽΪC4H8O2������3��
D.l mol D������̼�����Ʒ�Ӧ������������Ϊ22.4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ijNaOH�����к���NaCl���ʣ�Ϊ�ⶨ������ NaOH �������������������²���ʵ�飺
�� ���� 1.0g ��Ʒ����ˮ����� 250 mL ��Һ��
�� ȷ��ȡ 25.00 mL ������Һ����ƿ�У�
�� �μӼ��η�̪��Һ��
�� �� 0.10mol/L�ı�����ζ����Σ�ÿ����������������¼���£�
�ζ���� | ����Һ���(mL) | �����������Һ�����(mL) | |
�ζ�ǰ | �ζ��� | ||
1 | 25.00 | 0.50 | 20.60 |
2 | 25.00 | 6.00 | 26.00 |
3 | 25.00 | 1.10 | 21.00 |
��ش�
(1)����1.0g ��Ʒ����С�ձ���ҩ���⣬���õ�����Ҫ������_________��
(2)����Ʒ��� 250 mL ��Һ����С�ձ����������⣬�����õ��IJ���������_________��
(3)��_________�ζ���(������ʽ��������ʽ��)ʢװ 0.10mol/L �������Һ��
(4)�۲�ζ����յ�ʱ��Һ��ɫ�ı仯Ϊ_________��
(5)�ռ���Ʒ�Ĵ���Ϊ_________��
(6)����������������ⶨ���ƫ�ߵ���_________��
a���ζ�ǰ������ˮ��ϴ��ƿ
b��������ƿʱ������ƿ����Һ����
c�����ڵζ������в�����������Һ������ƿ��
d��ʢװ��Һ�ĵζ���ˮϴ��δ�ñ�Һ����ϴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�pH=2������һԪ��x��y�������Ϊ100mL��ϡ������pH����Һ����Ĺ�ϵ��ͼ��ʾ���ֱ�μ�NaOH��Һ���ζ��յ㣬����NaOH��Һ�����ΪVx��Vy����

A.xΪ���ᣬVx<VyB.xΪǿ�ᣬVx>Vy
C.yΪ���ᣬVx<VyD.yΪǿ�ᣬVx>Vy
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3�ֲ�ͬ�����£��ֱ����ݻ�Ϊ2L�ĺ����ܱ������г���2molA��1molB��������Ӧ:2A(g)+B(g)![]() 2D(g)��H=QkJ/mol��������������ݼ��±�:
2D(g)��H=QkJ/mol��������������ݼ��±�:
ʵ���� | ʵ��I | ʵ��II | ʵ��III |
��Ӧ�¶�/�� | 700 | 700 | 750 |
��ƽ��ʱ��/min | 40 | 50 | 30 |
n(D)ƽ��/mol | 1.5 | 1.5 | 1 |
��ѧƽ�ⳣ�� | K1 | K2 | K3 |
����˵����ȷ����
A. �����¶��ܼӿ췴Ӧ���ʵ�ԭ���ǽ����˷�Ӧ�Ļ�ܣ�ʹ����Ӱٷ������
B. ʵ��III��ƽ����������������䣬����������ͨ��1molA��1molD��ƽ�ⲻ�ƶ�
C. ʵ��III��ƽ��������ڵ�ѹǿ��ʵ��1��9/10��
D. K3>K2>K1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018��8��3���ҹ�ȷ�����������������顣Ŀǰij��Чҩ�����Ҫ�ɷ֡���������(����ʽΪC12H20O6)��һ�ֺϳ�·����ͼ��ʾ��
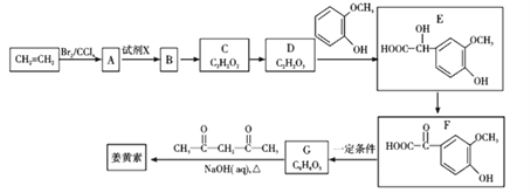
��֪��
��![]()
![]() CH3CHO+CO2��
CH3CHO+CO2��
��CH3CHO+
![]()
![]() +H2O
+H2O
�ش��������⣺
(1)A������Ϊ_________���Լ�XΪ_________��
(2)D�к��еĹ���������Ϊ_________��
(3)��ӦD��E�Ļ�ѧ����ʽΪ______________________________���䷴Ӧ������________��
(4)�����й�G(C8H8O3)����������ȷ����_________(����ȷ�𰸱��)��
a.����NaHCO3��Һ��Ӧ b.����Ũ��ˮ����ȡ����Ӧ
c.����FeCl3��Һ������ɫ��Ӧ d.l mol G�������3 mol H2�����ӳɷ�Ӧ
(5)�����صĽṹ��ʽΪ_________��
(6)G(C8H8O3)��ͬ���칹���У�д��ͬʱ�������������Ľṹ��ʽΪ_________��
�ٱ����ϵ�һȡ����ֻ��2�֣�
�ں˴Ź�����������4�����շ壻
��l mol���������ռ���Һ��Ӧ���������3 mol NaOH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����CO��H2����ȼ�ϼ״�(CH3OH)��һ���������ܱ������з�����Ӧ���������������ͼ��ʾ(��Ӧ����������̬)������˵���������
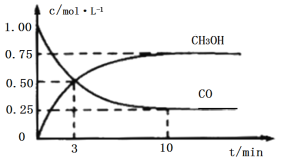
A.��Ӧ�Ļ�ѧ����ʽ��CO+2H2CH3OH
B.��Ӧ������3����ʱ�������淴Ӧ�������
C.��Ӧ��10���ӣ�(CO)=0.075mol/(L��min1)
D.��Ӧ��3���ӣ��ü״�����ʾ��Ӧ��ƽ������Ϊ![]() mol/(L��min1)
mol/(L��min1)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com