
【题目】某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在有图所示的装置中进行中和反应,通过测定反应过程中所放出的热量计算中和热.下列说法正确的是( ) 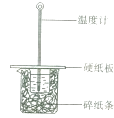
A.实验过程中没有热量损失
B.烧杯间填满碎纸条的作用是固定小烧杯
C.图中实验装置缺少环形玻璃搅拌棒
D.若将盐酸体积改为60mL,理论上所求中和热不相等
科目:高中化学 来源: 题型:
【题目】“轻轨电车”是近年来又一新兴的交通工具,具有无污染的优点.轻轨电车运行中,在轻轨电车跟架空电线的接触点上,由于高速摩擦会产生高温,因此接触点的材料应具有耐高温、不易氧化、能导电的性质.你认为最合适选作接触点的是( )
A.金刚石
B.石墨
C.铝
D.铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍.B的单质在D的单质中充分燃烧能生成其最高价化合物BD2 . E+与D2﹣具有相同的电子数.A的单质在F的单质中燃烧伴有苍白色火焰,产物溶于水得到一种强酸.回答下列问题:
(1)F的元素符号为 .
(2)A在周期表中的位置是 .
(3)A与D反应时,可以形成原电池,在原电池的负极上发生氧化反应的物质是 .
(4)B、D、E组成的一种盐中,E的质量分数为约43%,其俗名为 .
(5)E在D中燃烧产物的电子式为 .
(6)A与E可以形成离子化合物,该化合物与水反应的方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的常见化合价与原子序数的关系图: 
(1)元素F在周期表中的位置 .
(2)C2﹣、D+、G2﹣离子半径大小顺序是>>(用离子符号回答)
(3)C和G的氢化物中,沸点较低的是(用化学式回答),原因为 .
(4)C与E形成的化合物是(填“离子化合物”或“共价化合物”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用图1装置可以进行测定SO2转化为SO3的转化率的实验.已知SO3 的熔点是16.8℃,沸点是445.8℃.已知发生装置中所涉及反应的化学方程式为:Na2SO3(s)+H2SO4(98%)═Na2SO4+H2O+SO2↑ 
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置.请从图2A~E装置中选择最适合装置并将其序号填入下面的空格中. 
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是、、 .
(2)从乙处均匀通入O2 , 为使SO2 有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作是 .
(3)尾端球形干燥管的作用是 .
(4)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为%(用含a、b的代数式填写).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素x、y、z在元素周期表中的相对位置如图,下列推论合理的是( ) 
A.若y和z能形成化合物,则x为氮元素
B.若x、y、z的单质常温下都是气体,则Y为氧元素
C.若x、y、z是非金属元素,则它们气态氢化物的水溶液都显酸性
D.若x、y、z的原子序数之和小于20,则它们都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应过程的能量变化如图所示,下列说法正确的是( ) 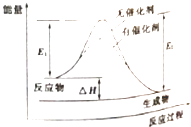
A.该反应能量变化类型与CaCO3分解反应相同
B.加催化剂后,正反应速率加快,逆反应速率减小
C.若该反应为氧化还原反应,则可以将其设计成原电池
D.反应热△H=E2﹣E1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属R原子的质量数为54,已知R离子含有28个中子,23个电子,由这种离子组成的化合物的化学式正确的是( )
A.RCl2
B.R3O4
C.R(OH)3
D.HRO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com