
| A、H2Y的电离方程式为:H2Y=2H++Y2- |
| B、在该酸式盐溶液中:[Na+]>[Y2-]>[HY-]>[OH-]>[H+] |
| C、HY-的水解方程式:HY-+H2O?H3O++Y2- |
| D、在该酸式盐溶液中:[Na+]>[HY-]>[OH-]>[H+]>[Y2-] |


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某烧碱溶液中含有少量杂质(不与盐酸反应),现用标准盐酸滴定NaOH溶液,测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用标准盐酸滴定NaOH溶液,测定其浓度.| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.80 | 25.30 |
| 2 | V | |||
| 3 | V | 6.00 | 31.35 | 25.35 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
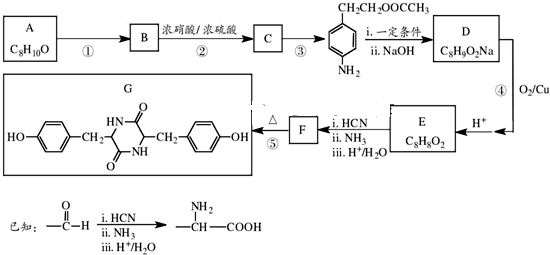
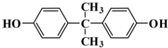 )与光气(
)与光气(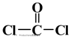 )聚合得到,请写出该聚碳酸酯的结构简式
)聚合得到,请写出该聚碳酸酯的结构简式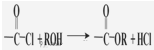 )
)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.4% | B、8.0% |
| C、16.3% | D、16.4% |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com