
【题目】短周期主族元素,a、b、c、d的原子序数依次增大。四种元素形成的单质依次为m、n、p、q;x、y、z是这些元素组成的二元化合物,其中z为形成酸雨的主要物质之一;25℃0.01mol·L-1w溶液中,![]() 。上述物质的转化关系如图所示。下列说法正确的是
。上述物质的转化关系如图所示。下列说法正确的是
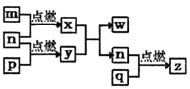
A. 原子半径的大小:a<b<c<d B. 氢化物的沸点:b>d
C. x的电子式为:![]() D. y、w含有的化学键类型完全相同
D. y、w含有的化学键类型完全相同
【答案】B
【解析】z是形成酸雨的主要物质之一,推出z是SO2,n、p为单质,因此n、p为S和O2, c(H+)/c(OH-)=10-10,溶液显碱性,即c(OH-)=10-2mol·L-1,w为强碱,即NaOH, 推出x和y反应可能是Na2O2与H2O反应,即n为O2,q为S,四种元素原子序数增大,推出a为H,b为O,p为Na,A、半径大小比较:一看电子层数,电子层数越多,半径越大,二看原子序数,电子层数相同,半径随着原子序数增大而减小,因此半径顺序是:Na>S>O>H,故错误;B、氢化物分别是H2O、H2S,H2O中含有分子间氢键,H2S没有,则H2O的沸点高于H2S,故正确;C、x为H2O,其电子式为:![]() ,故错误;D、y是过氧化钠,w为NaOH,前者只含离子键,后者含有离子键和共价键,故错误。
,故错误;D、y是过氧化钠,w为NaOH,前者只含离子键,后者含有离子键和共价键,故错误。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】已知:图甲是由某温度下![]() 、
、![]() 分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化图.图乙是常温下向100mL
分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化图.图乙是常温下向100mL![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液,混合溶液的pH变化图.如图所示与推测的结论相符的是
溶液,混合溶液的pH变化图.如图所示与推测的结论相符的是
图甲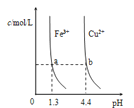 图乙
图乙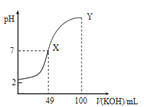
A.由图甲知:![]()
B.由图甲知:a、b点溶液中![]() ,b点的大
,b点的大
C.由图乙知:HA为强酸
D.由图乙知:Y点对应的溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范并能达到实验目的是
选项 | 实验操作 | 实验目的 |
A | 在一定条件下,向混有少量乙烯的乙烷中通入氢气 | 除去乙烷中的乙烯 |
B | 用玻璃棒蘸取待测液,点在干燥的pH试纸中部,片刻后与标准比色卡比较并读数 | 粗略测定NaClO溶液的pH |
C | 将0.1mol/LMgSO4溶液滴入到2mLNaOH溶液中至不再有沉淀生成,再滴入0.1mol/LCuSO4溶液 | 比较Mg(OH)2和Cu(OH)2的Ksp大小 |
D | 向亚硫酸钠溶液中滴加硝酸钡和稀硝酸 | 检验亚硫酸钠溶液是否变质 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是( )
A.已知:将Fe加入CuSO4 溶液中 Fe+ Cu2+= Cu + Fe2+
类推:将 Na加入 到CuSO4 溶液中2Na + Cu2+= Cu+2Na+
B.已知:稀硫酸与Ba(OH )2溶液反应至中性2H+ + SO4 2-+ Ba2++ 2OH- = BaSO4↓+ 2H2O
类推:NaHSO4 溶液与Ba(OH)2溶液反应至中性2H+ + SO4 2-+ Ba2++ 2OH- = BaSO4↓+ 2H2O
C.已知:铁和氯气反应2Fe + 3Cl2 ![]() 2FeCl3
2FeCl3
类推:铁和碘单质反应2Fe + 3I2 ![]() 2FeI3
2FeI3
D.已知:向Ca(ClO)2溶液中通入少量CO2:Ca2+ + 2ClO-+ CO2+ H2 O= CaCO3↓+2HClO
类推:向 Ca(ClO)2溶液中通入少量SO2:Ca2+ + 2ClO-+ SO2+ H2 O= CaSO3↓+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、材料等密切相关,下列叙述正确的是( )。
A.可用热的饱和碳酸钠溶液除去金属表面的矿物油
B.明矾溶于水会形成胶体,因此可用于自来水的杀菌消毒
C.煤经气化和液化两个化学变化过程,可变为清洁能源
D.“神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化中蕴含着丰富的化学知识。下列![]() 天工开物
天工开物![]() 的记载中不涉及合金的是
的记载中不涉及合金的是![]()
![]()
A.凡铸镜,模用灰沙,铜用锡和
B.凡倭铅![]() 锌
锌![]() 古书本无之,乃近世所立名色。其质用炉甘石
古书本无之,乃近世所立名色。其质用炉甘石![]() 主要成分为碳酸锌
主要成分为碳酸锌![]() 熬炼而成
熬炼而成
C.凡釜储水受火,日用司命系焉。铸用生铁或废铸铁器为质
D.凡治地生物,用锄、镈之属,熟铁锻成,熔化生铁淋口,入水淬健,即成刚劲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 600 | 800 | 830 | 1000 | 1200 |
K | 0.25 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K = 。
(2)该反应为 反应(选填“吸热”、“放热”)。反应达平衡后,若再通入一定量CO2,则平衡常数K将________,CO2的转化率________。(填“增大”、“减小”或“不变”)
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变 c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)若 600℃时,向容器中充入1mol CO、1mol H2O,反应达到平衡后,CO的转化率是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬渣(铬主要以Cr2O3形式存在,同时含有Al2O3、SiO2等杂质)是铬电镀过程中产生的含铬污泥,实现其综合利用,可减少铬产生的环境污染。铬渣综合利用工艺流程如下:
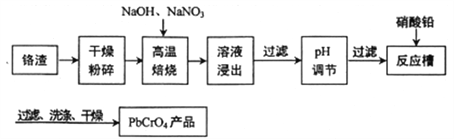
请回答下列问题:
(1)焙烧得到的产物含有Na2CrO4和一种无污染的气体,则生成Na2CrO4的反应方程式为________________________________________________________。
(2)除去铝元素的离子方程式为__________________________________________。
(3)理论上加入醋酸铅、硝酸铅均可以得到铬酸铅沉淀,工艺流程中不选用醋酸铅的原因是___________。
(4)铬酸铅是一种用于水彩和油彩的筑色颜料,遇到空气中的硫化物颜色会变黑,该过程的化学反应方程式为___________________________。
(5)实验室常利用Cr3+在碱性溶液中的还原性,使其转化为CrO42-,从而实现与Al3+的分离,这个过程中需要加入的两种试剂是__________、__________(填化学式),分离操作是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写和表示正确的是(△H的绝对值均正确)
A.2SO2(g)+O2(g)![]() 2SO3(g)△H=-196kJ/mol(反应热)
2SO3(g)△H=-196kJ/mol(反应热)
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol(燃烧热)
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热)
D.2NO2=O2+2NO△H=-116.2kJ/mol(反应热)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com