
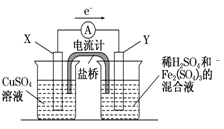
| | 正、负极判断 | 电极材料 | 电极反应式 |
| X极 | | | |
| Y极 | | | |
| | 正、负极判断 | 电极材料 | 电极反应式 |
| X极 | 负极 | 铜 | Cu-2e-===Cu2+ |
| Y极 | 正极 | 碳 | 2Fe3++2e-===2Fe2+ |
 a=0.01mol; b=0.02mol
a=0.01mol; b=0.02mol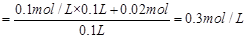 ,根据溶液中正负电荷守恒,可得
,根据溶液中正负电荷守恒,可得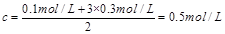


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
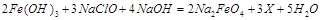 ,则X的化学式为 。
,则X的化学式为 。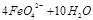

 。由此看来,高铁酸钠能够杀菌消毒是因为它具有 性,而能够除去水中悬浮物是因为 。
。由此看来,高铁酸钠能够杀菌消毒是因为它具有 性,而能够除去水中悬浮物是因为 。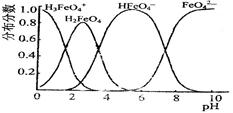

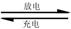
 则电池正极材料是 ,充电时电池正极 (填“得”“失”)电子,放电时电池的负极反应式为 。
则电池正极材料是 ,充电时电池正极 (填“得”“失”)电子,放电时电池的负极反应式为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.FeSO4 | B.H2SO4 | C.Fe2(SO4)3 | D.CuSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶解的铁粉为2.8g | B.原溶液中C(SO42-)=0.5mol/L |
| C.原混合溶液中C(H+)=1.2mol/L | D.原溶液中n(NO3-)=0.08mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
在空气中把铁灼烧至5000C就形成Fe3O4;温度再升高,可形成Fe2O3,在更高的温度下加热Fe2O3(约14000C)时,可失去氧,又得到Fe3O4。即: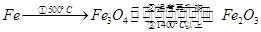 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2.8 g | B.5.6 g | C.11.2 g | D.1.4 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
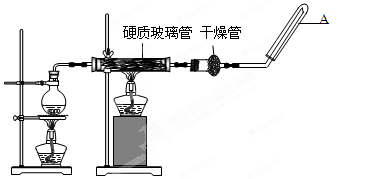
 ;
; 并指明该氧化还原反应的还原剂是 ,氧化剂是 。
并指明该氧化还原反应的还原剂是 ,氧化剂是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 化合物的性质。过程如下:
化合物的性质。过程如下: H)3具有两性,Cu(OH)2也具有两性吗?
H)3具有两性,Cu(OH)2也具有两性吗?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com