
| A. | 铜制水龙头 | B. | 铁制水龙头 | C. | 塑料水龙头 | D. | 陶瓷水龙头 |
分析 根据镀锌自来水管锈蚀最快,即与水龙头材料要形成原电池,并且镀锌自来水管中的锌和铁都要比水龙头材料活泼作负极,据此分析.
解答 解:镀锌自来水管与铜水龙头相连接,首先镀锌和铜以及自来水形成原电池,Zn的活动性强于Cu,金属Zn作负极,故使Zn锈蚀更快,表面的锌腐蚀了,里面的铁与Cu以及自来水又形成原电池,Fe的活动性强于Cu,金属铁作负极,故使Fe锈蚀更快;
铁制水龙头只能与镀锌以及自来水形成原电池,锌腐蚀了,里面的铁与铁制水龙头不能形成原电池;
塑料水龙头、陶瓷水龙头都不能形成原电池;
所以连接处自来水管锈蚀最快的是铜制水龙头;
故选A.
点评 本题考查了金属锈蚀的条件,完成此题,依据与水龙头材料要形成原电池,并且镀锌自来水管中的锌和铁都要比水龙头材料活泼作负极,腐蚀加快.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol Cl2作为氧化剂得到的电子数为NA | |
| B. | 在25℃,101kPa时,22.4L氢气中含有2NA个氢原子 | |
| C. | 14g氮气中含有7NA个电子 | |
| D. | NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15 mol/(L•S) | B. | 0.3 mol/(L•S) | C. | 0.6 mol/(L•S) | D. | 0.9 mol/(L•S) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、I-、NO3-、CO32- | B. | NH4+、Fe3+、OH-、Br- | ||
| C. | K+、Cl-、Cu2+、NO3- | D. | Al3+、SO42-、Na+、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素符号 | ② | ③ | ④ | ⑤ |
| 原子半径 | 130 | 118 | 75 | 73 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
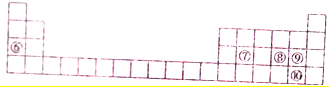
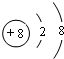 ;所给元素中,其含氧化合物能用于漂白,该元素可能是S、Cl(填元素符号)
;所给元素中,其含氧化合物能用于漂白,该元素可能是S、Cl(填元素符号)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2 L氧气中所含有的原子数为NA | |
| B. | 标准状况下,22.4LCCl4所含分子数为NA | |
| C. | 7.8g的Na2O2中含有的阴离子的数目为0.2NA | |
| D. | 27g Al分别与足量的稀硫酸及氢氧化钠溶液反应失去的电子数都是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH2+HCl→CH3CH2Cl | B. |  +HO-NO2$→_{55~60℃}^{浓H_{2}SO_{4}}$ +HO-NO2$→_{55~60℃}^{浓H_{2}SO_{4}}$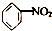 +H2O +H2O | ||
| C. | nCH2═CH2$\stackrel{一定条件}{→}$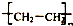 | D. | (C6H10O5)n+nH2O$\stackrel{一定条件}{→}$nC6H12O6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com