
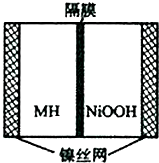
 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).该电池放电时的总反应为:MH+NiOOH=M+Ni(OH)2,下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).该电池放电时的总反应为:MH+NiOOH=M+Ni(OH)2,下列有关说法不正确的是( )| A. | 放电时负极反应为:MH+OH--e-→M+H2O | |
| B. | 电池的电解液可为KOH溶液,OH-向负极移动 | |
| C. | 放电时正极反应为:NiOOH+H2O-e-→Ni(OH)2+OH- | |
| D. | MH是一类储氢材料,其氢密度越大,电池的能量密度越高 |
分析 镍氢电池根据总反应:MH+NiOOH=M+Ni(OH)2 ,放电时,正极:NiOOH+H2O+e-=Ni(OH)2+OH-,负极:MH+OH--e-=M+H2O,以上式中M为储氢合金,MH为吸附了氢原子的储氢合金,据此分析解答.
解答 解:A、放电时负极反应为:MH+OH--e-=M+H2O,故A正确;
B、为了防止MH被氢离子氧化,镍氢电池中电解液为碱性溶液,主要为KOH作电解液,并且OH-向负极移动,故B正确;
C、放电时,正极:NiOOH+H2O+e-=Ni(OH)2+OH-,故C错误;
D、M为储氢合金,MH为吸附了氢原子的储氢合金,储氢材料,其氢密度越大,电池的能量密度越高,故D正确;
故选C.
点评 本题考查了原电池原理,明确题给信息的含义是解本题关键,难点的电极反应式的书写,题目难度中等.


科目:高中化学 来源: 题型:选择题
 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)$\frac{\underline{\;高温、高压\;}}{催化剂}$2NH3(g),673K、30MPa下,n(NH3)和n(H2)随时间t变化的关系如图所示.下列叙述中,正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)$\frac{\underline{\;高温、高压\;}}{催化剂}$2NH3(g),673K、30MPa下,n(NH3)和n(H2)随时间t变化的关系如图所示.下列叙述中,正确的是( )| A. | 点c处正反应速率和逆反应速率相等 | |
| B. | 点a处的正反应速率比点b处的大 | |
| C. | 点d(t1时)和点e(t2时)处n(N2)不同 | |
| D. | 在t2时,正反应速率大于逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
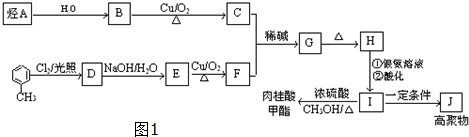
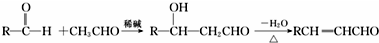
 ,J的结构简式为
,J的结构简式为 .
.
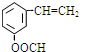 、
、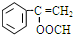 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3 | B. | 浓硫酸 | C. | NaCl | D. | NaNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,B为18电子分子,其结构式为
,B为18电子分子,其结构式为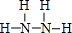 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2,H2S,O2 | B. | CH4,H2,CO | C. | NH3,H2,N2 | D. | HCl,Cl2,CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 | |
| B. | NaHSO3 溶液中,c(H2SO3)>c(SO32-),加水稀释后离子浓度均减小 | |
| C. | 加入少量NaOH溶液,$\frac{c(S{O}_{3}^{2-})}{c(HS{O}_{3}^{-})}$减小,$\frac{c(O{H}^{-})}{c({H}^{+})}$的值增大 | |
| D. | 加入氨水至中性,则c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:3 | B. | 3:2 | C. | 6:5 | D. | 4:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com