
【题目】25℃时,已知醋酸的电离常数为1.8×10-5。向20mL 2.0mol/LCH3COOH溶液中逐滴加入2.0mol/LNaOH溶液,溶液中水电离出的c(H+)在此滴定过程中变化曲线如下图所示。下列说法不正确的是

A. a点溶液中:c(H+)=6.0![]() 10-3mol
10-3mol![]() L-1
L-1
B. b点溶液中:c(CH3COOH)>c(Na+)>c(CH3COO-)
C. c点溶液中:c(OH-)=c(CH3COOH)+ c(H+)
D. d点溶液中:c(Na+)=2c(CH3COO-)+2c(CH3COOH)
【答案】B
【解析】
A.a点溶液没有加入NaOH,为醋酸溶液,根据电离平衡常数计算。设电离的出的H+的浓度为x,由于电离程度很低,可认为醋酸浓度不变。
CH3COOH![]() CH3COO-+H+
CH3COO-+H+
2 x x
Ka=![]() =
=![]() =1.8×10-5,解得x=6.0×10-3mol/L,A项正确;
=1.8×10-5,解得x=6.0×10-3mol/L,A项正确;
B.b点的溶液为CH3COOH和CH3COONa等浓度混合的溶液,物料守恒为c(CH3COOH) +c(CH3COO-)=2c(Na+),醋酸会电离CH3COOH![]() CH3COO-+H+,醋酸根会水解,CH3COO-+H2O
CH3COO-+H+,醋酸根会水解,CH3COO-+H2O![]() CH3COOH+OH-,水解平衡常数
CH3COOH+OH-,水解平衡常数![]() <1.8×10-5,CH3COOH的电离大于CH3COO-的水解,所以c(CH3COO-)> c(Na+)> c(CH3COOH);B项错误;
<1.8×10-5,CH3COOH的电离大于CH3COO-的水解,所以c(CH3COO-)> c(Na+)> c(CH3COOH);B项错误;
C.c点醋酸和氢氧化钠完全反应,溶液为CH3COONa溶液,在醋酸钠溶液中有电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),有物料守恒c(Na+)=c(CH3COO-)+c(CH3COOH),将两式联立得到质子守恒,则有c(OH-)=c(CH3COOH)+ c(H+);C项正确;
D.d点加入40mL的NaOH溶液,NaOH多一倍,为等物质的量浓度的NaOH和CH3COONa的混合溶液,有物料守恒c(Na+)=2c(CH3COO-)+2c(CH3COOH),D项正确;
本题答案选B。


科目:高中化学 来源: 题型:
【题目】氢气是未来非常理想能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O![]() 2H2+O2。制得的氢气可用于燃料电 池、合成氨工业。回答下列问题:
2H2+O2。制得的氢气可用于燃料电 池、合成氨工业。回答下列问题:
(1)分解海水时,__________能转变为_______________能。生成的氢气用于燃料电池时,___________能转变 为_____能。
(2)氢气可用于合成氨。一定温度下,向2L的密闭容器中加入1 molN2和3molH2 发生反应N2(g)+3H2(g)![]() 2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的
2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的![]() 。则前2min用NH3表示的化学反应速率为__________;平衡时,N2的转化率为_________。
。则前2min用NH3表示的化学反应速率为__________;平衡时,N2的转化率为_________。
(3)合成氨还需要大量的氮气为原料,工业上获得大量氮气的方法是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下把V体积氨气溶于1体积水中得到氨的饱和溶液,试完成下列填空。
(1)NH3通入水中发生的反应为____________________。
(2)氨水中存在的分子有__________________________。
(3)氨水中存在的离子有__________________________。
(4)所得氨水的质量分数为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国高校目前联合研究一种稀土制冷材料,其主要成分是LaCaMnO.
(1)猛原子的基态价层电子排布式为__.
(2)S与O为同主族元素,其中电负性较大的是__; H2S分子中S原子杂化轨道类型为__;试从结构角度解释H2SO4的酸性大于H2SO3的酸性:__.
(3)据报道,Ca在空气中点燃生成CaO和少量Ca2N2.
①Ca2N2和水反应生成NH2﹣NH2,NH2﹣NH2能否作配体?__(填“能”或“否”)
②CaO形成的晶体与NaCl晶体一样,为面心立方最密堆积,则一个CaO晶胞中含 有Ca2+数为__;欲比较CaO与NaCl的晶格能大小,需考虑的数据是__.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在某密闭容器中发生反应:2HI(g)![]() H2(g)+I2(g) ΔH>0,若15s内c(HI)由0.1mol·L-1降到0.07mol·L-1,则下列说法正确的是( )
H2(g)+I2(g) ΔH>0,若15s内c(HI)由0.1mol·L-1降到0.07mol·L-1,则下列说法正确的是( )
A. 0~15 s内用I2表示的平均反应速率为v(I2)=0.002 mol·L-1·s-1
B. c(HI)由0.07 mol·L-1降到0.05 mol·L-1所需的反应时间小于10 s
C. 升高温度正反应速率加快,逆反应速率减慢
D. 减小反应体系的体积,化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在水溶液中的电离方程式正确的是( )
A. NaHSO4 = Na++ HSO4-B. BaSO4 = Ba2++SO42-
C. CH3COONH4![]() NH4+ + CH3COO-D. H2CO3
NH4+ + CH3COO-D. H2CO3![]() 2H++CO32-
2H++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。下面列出了几组物质,请将物质的合适组号填写在空格上。
A.金刚石与石墨;B.氕与氘;C.甲烷与戊烷;D.![]() 与
与 ;E.
;E.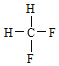 与
与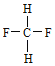 。
。
(1)同素异形体___;(2)同系物___;(3)同分异构体___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)利用VSEPR推断分子或离子的空间构型。
PO![]() __________;CS2____________;AlBr3(共价分子)__________。
__________;CS2____________;AlBr3(共价分子)__________。
(2)有两种活性反应中间体粒子,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给出的这两种粒子的球棍模型,写出相应的化学式:
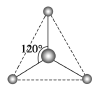 ______________;
______________;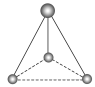 ______________。
______________。
(3)按要求写出第二周期非金属元素构成的中性分子的化学式。
平面三角形分子________,三角锥形分子________,四面体形分子________。
(4)为了解释和预测分子的空间构型,科学家在归纳了许多已知的分子空间构型的基础上,提出了一种十分简单的理论模型——价层电子对互斥模型。这种模型把分子分成两类:一类是____________________;另一类是____________________。
BF3和NF3都是四个原子的分子,BF3的中心原子是________,NF3的中心原子是________;BF3分子的立体构型是平面三角形而NF3分子的立体构型是三角锥形的原因是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用如下装置制备乙酸乙酯。下列有关分析不正确的是

A. b中导管不能插入液面下,否则会阻碍产物的导出
B. 固体酒精是一种白色凝胶状纯净物,常用于餐馆或野外就餐
C. 乙酸乙酯与![]() 互为同分异构体
互为同分异构体
D. 乙酸、水、乙醇羟基氢的活泼性依次减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com