
(10分)A~H是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知B、D是生活中常见的金属单质,G是气体单质,C的焰色反应呈黄色。

请回答下列问题:
(1)元素B在周期表中的位置是 ,C的电子式为 ,H的结构式为 。
(2)反应①的化学方程式为 。
(3)A与盐酸反应的离子方程式为 。
(4)F溶液显 (填“酸性”、“中性”或“碱性”),原因是 (用离子方程式表示)。
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
(10分) A、B、C、D、E是位于短周期的主族元素。已知:① 热稳定性:H m D > H m C;② C m-、E (m-1)- 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
(1) HmDm的电子式_____________。
(2) 还原性强弱:C m- ___ E (m-1)- (填“>”或“<”);能证明其还原性强弱的离子方程式为:_____ ___。
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:____________________。
(4) 常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的离子方程式 。在该溶液中溶质中含有的化学键类型是 。
(5) 在A、B、C、E单质中,符合下列转化关系的是_____________(填元素符号)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省通许县丽星中学高二下学期期末考试化学试卷(带解析) 题型:填空题
(10分)配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是________。
| A.CO2 | B.H3O+ | C.CH4 | D.NH4+ |
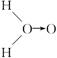 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)查看答案和解析>>
科目:高中化学 来源:2013届河北省高二下学期三调考试化学试卷(解析版) 题型:填空题
(共10分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
|
A |
|
|
|||||||||||||||
|
B |
|
|
|
C |
D |
E |
F |
|
|||||||||
|
G |
H |
I |
J |
|
K |
L |
|
||||||||||
|
|
|
|
|
|
M |
|
N |
|
|
|
|
|
|
|
|
|
|
试回答下列问题:
(1)请写出元素N的基态原子电子排布式 。
(2)D的氢化物易溶于水的原因
(3)D和E的电负性的大小: > (用元素符号表示)
(4)由A、C、D形成的ACD分子中,含有 个σ键, 个π键。
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
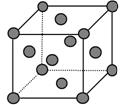
①与M同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有 __________(填元素符号),其中一种金属的晶胞结构如图所示,该晶胞中含有金属原子的数目为 。
②MO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是__________(填“极性”或“非极性”)分子。
③在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有___________(填序号),CS2分子的空间构型是__________。
查看答案和解析>>
科目:高中化学 来源:2014届四川省高一下学期期中考试化学试卷(解析版) 题型:填空题
(10分) A、B、C、D、E是位于短周期的主族元素。已知:① 热稳定性:H m D > H m C;② C m-、E (m-1)- 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
(1) HmDm的电子式_____________。
(2) 还原性强弱:C m- ___ E (m-1)- (填“>”或“<”);能证明其还原性强弱的离子方程式为:_____ ___。
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:____________________。
(4) 常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的离子方程式 。在该溶液中溶质中含有的化学键类型是 。
(5) 在A、B、C、E单质中,符合下列转化关系的是_____________(填元素符号)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com