
下列离子方程式书写正确的是( )
A. 石灰石溶于盐酸:CO32﹣+2H+═H2O+CO2↑
B. Al2O3粉末溶于NaOH溶液中:Al2O3+2OH﹣=2AlO2﹣+H2O
C. 硫酸氢钠溶液与氢氧化钡溶液的反应:Ba2++SO42﹣=BaSO4↓
D. 氧化钠加入盐酸中:O2﹣+2H+═H2O
考点: 离子方程式的书写.
专题: 离子反应专题.
分析: A.碳酸钙不溶于水,在离子反应中应保留化学式;
B.Al2O3粉末溶于NaOH溶液反应生成偏铝酸钠和水;
C.漏写生成水的离子反应;
D.氧化钠在离子反应中应保留化学式.
解答: 解:A.石灰石溶于盐酸的离子反应为CaCO3+2H+═H2O+CO2↑+Ca2+,故A错误;
B.Al2O3粉末溶于NaOH溶液中的离子反应为Al2O3+2OH﹣=2AlO2﹣+H2O,故B正确;
C.硫酸氢钠溶液与氢氧化钡溶液的反应,若硫酸氢钠少量时的离子反应为:H++OH﹣+Ba2++SO42﹣=BaSO4↓+H2O,故C错误;
D.氧化钠加入盐酸中的离子反应为Na2O+2H+═H2O+2Na+,故D错误;
故选B.
点评: 本题考查离子反应方程式的书写,明确发生的化学反应及离子反应方程式的书写方法即可解答,题目难度不大.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
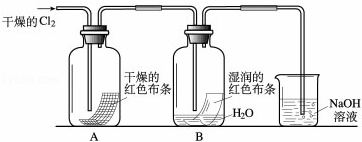
为了探究HClO的漂白性,某同学设计了如下的实验.
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是 ;从集气瓶B中湿润的红色布条的现象可得出的结论是 .
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是 .
(3)烧杯中溶液所起的作是 .
(4)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2mol•L﹣1的NaOH溶液的体积至少应为多少?(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
若原子核外电子的排布的基本规律为最外层电子数不超过5个,次外层电子数不超过10个,倒数第三层电子数不超过15个,而各电子层电子的最大容量仍为2n2,则元素周期表中第三、第四、第五周期含有的元素分别有( )
A. 5种、10种、15种 B. 8种、18种、18种
C. 8种、10种、15种 D. 9种、10种、15种
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定质量的铁、氧化铁、氧化铜的混合物粉末放入70mL 4.0mol/L盐酸中,充分反应后产生448mL H2(标准状况),残留固体0.64g.过滤,滤液中无Cu2+.将滤液加水稀释到200mL,测得其中c(H+)为0.20mol/L.则原混合物中单质铁的质量是( )
A. 2.80g B. 3.25g C. 3.36g D. 4.48g
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液只含有Na+,Al3+,Cl﹣,SO42﹣四种离子,已知Na+,Al3+,Cl﹣的个数比为3:2:1.则溶液中Al3+与SO42﹣离子的个数比为( )
A. 1:2 B. 1:4 C. 3:4 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
化学和材料开发制造、科学研究、生产生活等密切相关.
(1)第十八届江苏省运动会于2014年9月19日在徐州奥体中心开幕,奥体中心建筑采用了世界领先的钢结构技术,建筑材料中还使用了大量的铝合金、玻璃等.
①工业上铁的冶炼是在 中进行的,主要原料有铁矿石,焦炭、空气、 等.
②下列有关铝合金性能的叙述正确的是 c (填字母).
a.密度大 b.强度小 c.耐腐蚀
③下列物质中,不是工业上制造玻璃的主要原料的是 (填字母).
a.水玻璃 b.二氧化硅 c.碳酸钠
(2)化工生产和科学研究中,经常需要配制一定物质的量浓度的溶液.
①在实验室,使用容量瓶来准确配制 、一定浓度的溶液.
②欲配制1.00mol/L的氯化钠溶液100mL,用不到的仪器是 (填“烧杯”、“玻璃棒”或“分液漏斗”).配制500mL0.l mol/L氢氧化钠溶液需要氢氧化钠的质量是 g.
③在溶液稀释前后,溶液的体积发生了变化,但溶液中 的物质的量不变.配制一定物质的量浓度的Na2CO3溶液时,下列操作正确的是 (填字母).
a.将称好的固体在烧杯中溶解,所得溶液冷至室温再转移到容量瓶中
b.定容时,如果加水超过了刻度线,用胶头滴管直接吸出多余的部分
c.定容摇匀后发现溶液液面低于刻度线,再补加少量蒸馏水至刻度线
(3)物质的结构决定物质的性质,物质的性质关系到物质的用途.
①以电解 为基础制备氯气等产品的工业称为氯碱工业.在实验室要将氯化钠溶液和氯化钾溶液区别开来,可以采用的方法是 .
②当分散剂是水或其他液体时,根据 直径大小的不同,可以将分散系分为浊液、胶体和溶液.在实验室区分胶体与溶液常用的一种物理方法为 .
③在生产中,人们曾用浓氨水来检验氯气管道是否漏气.如果氯气管道某处漏气,用浓氨水检查时就会产生白烟的现象,又知此时发生的是有氮气生成的置换反应,则此时发生反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
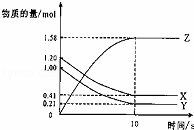
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
|
| A. | 反应开始到10s,用Z表示的反应速率为 0.158mol/(L•s) |
|
| B. | 反应开始到10s,X的物质的量浓度减少了0.79mol/L |
|
| C. | 反应开始到10s时,Y的反应速率为0.0395mol/(L•s) |
|
| D. | 反应的化学方程式为:X(g)+Y(g)⇌Z(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
将51.2g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500mL 2mol/L NaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO2的物质的量为( )
A. 0.2mol B. 0.6mol C. 0.8mol D. 1.0mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com