
| A、加入足量稀HNO3酸化的AgNO3溶液 |
| B、先加入足量BaCl2溶液,过滤,再加入AgNO3溶液 |
| C、先加入足量稀H2SO4,再加入AgNO3溶液 |
| D、先加入稀盐酸,再加入AgNO3溶液 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
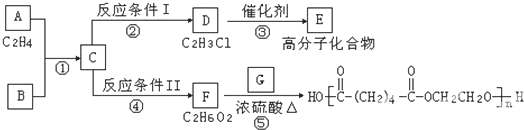
查看答案和解析>>
科目:高中化学 来源: 题型:

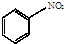
| Fe |
| HCl |
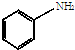
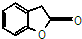 和
和 ,鉴别I和J的试剂为
,鉴别I和J的试剂为 )制得.请写出以L为原料制得M的合成路线流程图(无机试剂任用).流程图示例如下:
)制得.请写出以L为原料制得M的合成路线流程图(无机试剂任用).流程图示例如下:| HBr |
| NaOH溶液 |
| △ |
 )→
)→查看答案和解析>>
科目:高中化学 来源: 题型:
| A、漂白精的有效成分是Ca(ClO)2 |
| B、利用高纯硅的半导体性能,可以制成光电池 |
| C、NO、NO2是大气污染物,能在空气中稳定存在 |
| D、HCl、NH3、BaSO4都是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、③④①② |
| C、④①③② | D、②①④③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
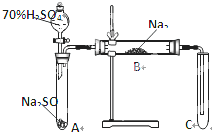 类比思想是化学学习常用的方法.已知Na2O2能与CO2反应,甲同学受到启发,提出一个相似的观点:Na2O2与SO2也能够反应.该同学用下图所示的装置进行实验,充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.
类比思想是化学学习常用的方法.已知Na2O2能与CO2反应,甲同学受到启发,提出一个相似的观点:Na2O2与SO2也能够反应.该同学用下图所示的装置进行实验,充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(H2)=0.3 mol?L-1?min-1 |
| B、v(N2)=0.2 mol?L-1?min-1 |
| C、v(NH3)=0.25 mol?L-1?min-1 |
| D、v(H2)=0.4 mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝热反应属于吸热反应 |
| B、若某反应的反应物的总能量大于生成物的总能量,则该反应为吸热反应 |
| C、H2→H+H的变化需要吸收能量 |
| D、吸热反应是指需要加热才能进行的反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com