
(1)钢铁工业对促进经济和社会发展起了重要作用。
①不锈钢含有的Cr元素是在炼钢过程的氧吹 (填“前”或“后”)加入。
②炼钢时,加入硅、锰和铝的目的是 。
③炼铁和炼钢生产中,尾气均含有的主要污染物是 。从环保和经济角度考虑,上述尾气经处理可用作 。
(2)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式: ;
②写出“联合制碱法”有关反应的化学方程式: ;
③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同? 。
(1)①后(1分)②脱氧和调整钢的成分(2分)③ CO (2分) 燃料(或还原剂)(2分)(2)① 2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O (2分)
2NH3↑+CaCl2+2H2O (2分)
② NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl (2分)
2NaHCO3 Na2CO3+CO2↑+H2O (2分)
Na2CO3+CO2↑+H2O (2分)
(或写总反应方程式:2NaCl+2NH3+CO2+H2O=Na2CO3+2NH4Cl)
③“氨碱法”CO2来源于灰石煅烧,“联合制碱法”CO2来源于合成氨工业的废气;(2分)
解析试题分析:(1)①因为Cr易被氧化,若氧吹前加入Cr会形成炉渣被除去;②加入硅、锰和铝的目的是脱氧和调整钢的成分③主要污染物是CO,故可用作燃料或还原剂;(2)“氨碱法”需要先制取氨气,故氯化钙来源于2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O;②联合制碱法是先向氯化钠的饱和溶液中通入氨气,再通过二氧化碳制得碳酸氢钠晶体,过滤出来加热得碳酸钠;③“氨碱法”CO2来源于石灰石煅烧,“联合制碱法”CO2来源于合成氨工业的废气。
2NH3↑+CaCl2+2H2O;②联合制碱法是先向氯化钠的饱和溶液中通入氨气,再通过二氧化碳制得碳酸氢钠晶体,过滤出来加热得碳酸钠;③“氨碱法”CO2来源于石灰石煅烧,“联合制碱法”CO2来源于合成氨工业的废气。
考点:考查炼钢的过程和制碱的原理


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:单选题
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
下列有关说法正确的是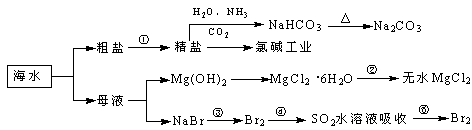
| A.过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.用澄清的石灰水可鉴别NaHCO3和Na2CO3 |
| C.过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2 |
| D.工业上通过电解饱和MgCl2溶液制取金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是
| A.海水中含有溴元素,只需经过物理变化就可以得到溴单质 |
| B.海水蒸发制海盐的过程中只发生了化学变化 |
| C.从海水中可以得到MgCl2,电解熔融MgCl2可制备Mg |
| D.利用潮汐发电是将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
[化学—选修2化学与技术](15分)
(1)下列关于工业生产说法正确的是 。(填序号)
| A.在侯氏制碱工业中,向饱和氯化钠溶液中先通二氧化碳,后通氨气 |
| B.在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率 |
| C.在氯碱工业,电解槽被离子交换膜隔成阴极室和阳极室 |
| D.工业上采用电解熔融氯化铝的方法制取金属铝 |
| pH | Ca2+ 、Mg2+总浓度 | 细菌总数 |
| 6.5~8.5 | < 0.004 5 mol·L-1? | <100个·mL-1? |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(11分)从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(一)海水淡化的方法主要有 (只填一种)。
(二)从海水中提取溴和镁的流程如下图所示:
(1)提取Br2时,第一次通入Cl2后发生反应的离子方程式是 ;
②中SO2表现 (填“氧化”或“还原”)性;
第二次通入Cl2后,要提取Br2还要进行的操作为 。
(2)为了实现对镁离子的富集,①中加入的足量试剂是 (填化学式);
请从节约能源,提高金属镁的纯度分析,以下最适宜的冶炼的方法是
(填字母)。
A.Mg(OH)2 MgO MgO  Mg Mg |
B.Mg(OH)2  MgO MgO  Mg Mg |
C.Mg(OH)2 无水MgCl2 无水MgCl2 Mg Mg |
D.Mg(OH)2 MgCl2(溶液) MgCl2(溶液) Mg Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:
(1)请列举海水淡化的两种方法:________、________。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、________、________或H2、________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为_____________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式 ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是____________。
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图:
请你参与分析讨论:
①图中仪器B的名称:________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是___________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:____。
④C中液体产物颜色为________。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上对海水资源综合开发利用的部分工艺流程如下图所示。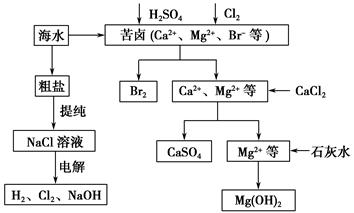
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽。离子膜和隔膜均允许通过的分子或离子是________。电解槽中的阳极材料为____________。
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备?__________,原因是______________________________
(3)溴单质在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
地球的海水总量约有1.4×1018t,是人类最大的资源库。
(1)如图利用海水得到淡水的方法为 。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如下图。a是电源的 极;Ⅰ口排出的是 (填“淡水” 或“浓水”)。
(3)海水淡化后的浓水中含大量盐分(主要含有Mg2+、Ca2+、Fe3+和SO42-),排入水中会改变水质,排到土壤中会导致土壤盐碱化,故不能直接排放,可以与氯碱工业联产。
电解前需要把浓水精制,所需试剂主要包括:HCl、NaOH、BaCl2、Na2CO3等),其中HCl的作用主要是 。
(4)铀是核反应最重要的燃料,其提炼技术直接关系着一个国家核工业或核武器的发展水平,海水中铀以UCl4形式存在(以离子形式存在),每吨海水只含3.3毫克铀,海水总量极大,铀总量相当巨大。不少国家正在探索海水提铀的方法。现在,已经研制成功一种螯合型离子交换树脂,它专门吸附海水中的铀,而不吸附其他元素。其反应原理为:___________________________(树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为:________________________。
(5)离子交换树脂法是制备纯水(去离子水) 的主要方法。某阳离子交换树酯的局部结构可写成(如图)。该阳离子交换树脂是由单体苯乙烯和交联剂对二乙烯基苯聚合后再经 反应得到的。自来水与该离子交换树脂交换作用后显 (填“酸性”、“碱性”或“中性”)。
(6)中国《生活用水卫生标准》中规定,水的总硬度不能过大。如果硬度过大,饮用后对人体健康与日常生活有一定影响。暂时硬水的硬度是由 (填阴离子符号)引起的,经 (填操作名称)后可被去掉。永久硬水的硬度可由离子交换法去掉。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金维生素”。工业上回收废钒催化剂(含有V2O5、VOSO4、K2SO4、SiO2)中钒的主要流程如下: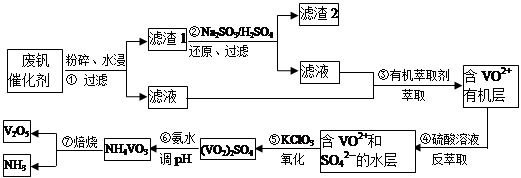
已知:(1)V2O5和NH4VO3均为难溶物,VOSO4和(VO2)2SO4均为易溶物。
(2) 2VO2++H2C2O4+2H+ = 2VO2+ + 2CO2↑+ 2H2O
回答下列问题:
(1)步骤①前,粉碎的目的是_________________________。
(2)步骤②中发生反应的离子方程式为__________________________。
(3)步骤③的变化过程可简化为(HA表示有机萃取剂):
VOSO4 (水层)+ 2HA(有机层) VOA2(有机层)+ H2SO4(水层),则步骤④中可选择硫酸作反萃取的原因是_____________。
VOA2(有机层)+ H2SO4(水层),则步骤④中可选择硫酸作反萃取的原因是_____________。
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定操作⑤后溶液中含钒量的步骤为:取10.0mL0.1mol/LH2C2O4溶液于锥形瓶中,加入指标剂,将待测液盛放在滴定管中,滴定到终点时,消耗待测液的体积为10.0mL,由此可知(VO2)2SO4溶液钒元素的含量为_________g/L。
(5)V2O5可用金属(如Ca、Al)热还原法获得钒,则金属铝热还原制得钒的化学方程式为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com