
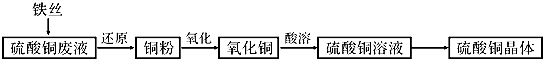
���� ����˿������ͭ��Һ���������������ͱ��л�����Ⱦ�ķ�ͭ���Ʊ�����ͭ������������̣���������Ͷ������ͭ�У������û�������ͭ������ͭ���Ժ������������·�����Ӧ��������ͭ����ͭ�к��е��л����ʺ���̼Ԫ�أ����ջ����̼���ʻ���CO�����л�ԭ�ԣ����Ժ�����ͭ�ڼ����·�����Ӧ���õ�����ͭ��������ͭ���Ժ����ᷴӦ�õ�����ͭ��Һ��
��1������ͭ����ɱ�����������ؽ���������ͭ��ʹ�����ʱ��Ե����ʣ�
��2�������������������Ժ����ᷴӦ��
��3����ɫ��ĩ����ϡ������Һ����Һ������������ɫ��ζ���壬������Ϊ������̼����ɫ��ĩΪ��ʽ̼��ͭ��
��4������ͭ���Ժ�Ũ�����ڼ��ȵ������·�����Ӧ�õ�����ͭ��ˮ�Լ���������
��5����ʯī�缫�������ͭ��Һ������Ϊ���������ӷŵ磻
��6�����ݳ����ܽ�ƽ����ܶȻ��������㣮
��� �⣺����˿������ͭ��Һ���������������ͱ��л�����Ⱦ�ķ�ͭ���Ʊ�����ͭ������������̣���������Ͷ������ͭ�У������û�������ͭ������ͭ���Ժ������������·�����Ӧ��������ͭ����ͭ�к��е��л����ʺ���̼Ԫ�أ����ջ����̼���ʻ���CO�����л�ԭ�ԣ����Ժ�����ͭ�ڼ����·�����Ӧ���õ�����ͭ��������ͭ���Ժ����ᷴӦ�õ�����ͭ��Һ��
��1������ͭ����ɱ�����������ؽ���������ͭ��ʹ�����ʱ��Ե����ʣ�
�ʴ�Ϊ����ʹ�����ʱ��ԣ�
��2������˿��Ͷ������ͭ��Һǰ����ϡH2SO4���д�����Ŀ���dz�ȥ���⣬�����ķ�Ӧ�����У�Fe2O3+6H+�T2Fe3++3H2O��
�ʴ�Ϊ��Fe2O3+6H+�T2Fe3++3H2O��
��3����ɫ��ĩ����ϡ������Һ����Һ������������ɫ��ζ���壬������Ϊ������̼����ɫ��ĩΪ��ʽ̼��ͭ�� Cu2�� OH��2CO3����
�ʴ�Ϊ��Cu2�� OH��2CO3��
��4����ϡ����������������ͭ������������ͭ����Ӧ�Ļ�ѧ��Ӧ����ʽΪ2Cu+O2+2H2SO4�T2CuSO4+2H2O��
�ʴ�Ϊ��2Cu+O2+2H2SO4�T2CuSO4+2H2O��
��5����ʯī�缫�������ͭ��Һ������Ϊ���������ӷŵ磬��������ӦʽΪ��4OH--4e-=2H2O+O2����
�ʴ�Ϊ��4OH--4e-=2H2O+O2����
��6������Һ��pH=8ʱ��c��H+��=10-8mol/L��c��OH-��=10-6mol/L��Ksp[Cu��OH��2]=c��Cu2+����c2��OH-��=2.2��10-20��c��Cu2+��=2.2��10-8mol/L��
�ʴ�Ϊ��2.2��10-8��
���� ������һ�����ʵķ�����ᴿ��ʵ�鷽������⣬�漰����ʽ��д���缫��Ӧʽ��д����ҺpH���ܶȻ��ļ��㣬����ѧ�������ͽ��������������Ѷ��еȣ�


 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ú˴Ź���������1-������2-����� | |
| B�� | �ð�ˮ����Al3+��Mg2+��Ag+ | |
| C�� | ��Ba��NO3��2��Һ����Cl-��SO42-��CO32- | |
| D�� | ��KMnO4������Һ�����������ͱ�ȩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
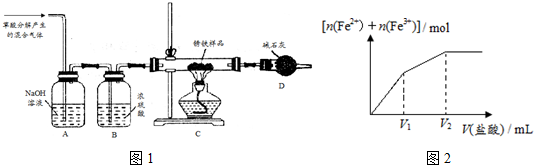
 ij��ȤС����Ƴ���ͼװ�ã��������Ѽ�飩����֤ͭ��ϡ���ᷴӦ�IJ����֪��FeSO4+NO�T[Fe��NO��]SO4���÷�Ӧ�ϻ�����������һ����[Fe��NO��]2+ʱͻ��������ɫ��
ij��ȤС����Ƴ���ͼװ�ã��������Ѽ�飩����֤ͭ��ϡ���ᷴӦ�IJ����֪��FeSO4+NO�T[Fe��NO��]SO4���÷�Ӧ�ϻ�����������һ����[Fe��NO��]2+ʱͻ��������ɫ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��Mg��Al | B�� | Al��Mg��Na | C�� | Mg��Al��Na | D�� | Na��Al��Mg |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�� | B�� | ����һԪ�� | C�� | ����һԪȩ | D�� | ����һԪ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ | B�� | ��Ϊ��ɫ���� | ||
| C�� | ���Ⱦ��ֽ� | D�� | ��ˮ��Һ����ʹ��̪��Һ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֬û�й̶����۵�ͷе㣬��֬�ǻ���� | |
| B�� | ��Ȼ��֬������ɻ���������ӹ��ɵĻ���� | |
| C�� | ��֬����Ҫ�ɷ��Ǹ�֬����ĸ�������������һ�� | |
| D�� | ����ˮ����ȡ�����ֲ��������ȡ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com