
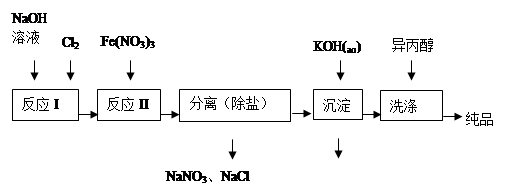
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
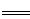 2Fe3++8SO42-(2分)
2Fe3++8SO42-(2分) ,c(OH-)=1.0×10-11,c(H+)=1.0×10-3,pH= 3;
,c(OH-)=1.0×10-11,c(H+)=1.0×10-3,pH= 3; 2K2FeO4+3KNO2+2H2O,N元素化合价降低,是氧化剂,铁的化合价降低,是还原剂,氧化剂与还原剂的物质的量之比为3﹕1,
2K2FeO4+3KNO2+2H2O,N元素化合价降低,是氧化剂,铁的化合价降低,是还原剂,氧化剂与还原剂的物质的量之比为3﹕1, 2Fe3++8SO42-。
2Fe3++8SO42-。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源:不详 题型:单选题
| A.6.4 g | B.4.8 g | C.2.4 g | D.1.6 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe | B.FeO | C.Fe(OH)3 | D.Fe2O3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

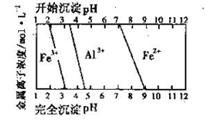

 FeCO3(s)+H2CO3(aq)的平衡常数为_______。
FeCO3(s)+H2CO3(aq)的平衡常数为_______。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在反应后的溶液中滴加KSCN溶液,溶液呈红色 |
| B.反应后溶液中c(Cl-)=6mol/L |
| C.反应后溶液中加入铁屑不溶解 |
| D.反应后溶液中c(Cu2+): c(Fe2+)=1:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Cu2++Cu。由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。一同学对某次用氢气还原氧化铜实验所得的红色固体产物作了验证,实验操作和实验现象记录如下:
Cu2++Cu。由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。一同学对某次用氢气还原氧化铜实验所得的红色固体产物作了验证,实验操作和实验现象记录如下:| 加入 试剂 | 稀硫酸 | 浓硫酸、 加热 | 稀硝酸 | 浓硝酸 |
| 实验 现象 | 红色固体和 蓝色溶液 | 无色气体 | 无色气体和 蓝色溶液 | 红棕色气体 和蓝色溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
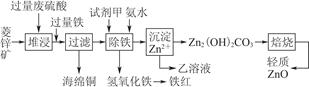
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.3 | 9.7 |
| Fe3+ | 1.5 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.赤铁矿的主要成分是Fe3O4 |
| B.钢铁在湿空气中生锈,生成Fe2O3和H2 |
| C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加铁粉,然后过滤 |
| D.Fe3+与KSCN反应产生红色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com