
| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| C. | 1.00 mol NaCl中含有6.02×1023个NaCl分子 | |
| D. | 纯净矿泉水、铝热剂、漂白粉均为混合物 |
科目:高中化学 来源: 题型:解答题
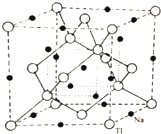 ⅢA族的硼、铝、镓、铟、铊等元素在化合物中通常表现出+3价,含ⅢA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题.
ⅢA族的硼、铝、镓、铟、铊等元素在化合物中通常表现出+3价,含ⅢA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

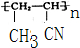
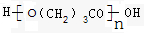
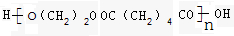 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两溶液中c(OH-):①=② | |
| B. | 两溶液的物质的量浓度:①=② | |
| C. | 两溶液分别加水稀释10倍,稀释后溶液的pH:①>② | |
| D. | 等体积的两溶液分别与同浓度的盐酸完全中和,消耗盐酸的体积:①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24LCl2溶于足量水中转移电子的数目为0.1NA | |
| B. | 标准状况下,22.4L苯中含有双键的数目为3NA | |
| C. | 常温下,16gO2和O3的混合气体中含有氧原子的数目为NA | |
| D. | 25℃时,pH=1的醋酸溶液中含有H+的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
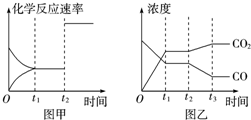
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 处理废弃物 | B. | 治理污染点 | C. | 减少有毒物排放 | D. | 杜绝污染源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通常状况下,NO2是红棕色的气体 | |
| B. | 氯水光照久置后最终变为稀盐酸 | |
| C. | 氯化钙溶液和AgNO3溶液混合有白色沉淀产生 | |
| D. | 加热时,铁单质与浓硝酸不发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com