
【题目】设NA为阿伏加罗常数的值,下列叙述正确的是( )
A.在标况下,11.2 L NO与11.2 L O2混合后所含分子数为0.75NA
B.常温常压下,16gO3所含的电子数为8NA
C.5NH4NO3 ![]() 2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA
D.铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA
科目:高中化学 来源: 题型:
【题目】著名化学家徐光宪获得“国家最高科学技术奖”,以表彰他在稀土萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法不正确的是( )
A. 铈(Ce)元素在自然界中主要以化合态形式存在
B. 铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI = CeI4 + 2H2↑
C. 用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+ = Ce3++Fe3+
D. 四种稳定的核素![]() 、
、![]() 、
、![]() 、
、![]() ,它们互称为同位素
,它们互称为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含氮污染物的治理是环保的一项重要工作。合理应用和处理氮的化合物,在生产生活中有重要意义。
I.污染物SO2、NOx经O2预处理后用CaSO3悬浊液吸收,可减少尾气中SO2、NOx的含量。T℃时,O2氧化烟气中SO2、NOx的主要反应的热化学方程式为:

(1) T℃时,反应3NO(g)+O3(g)![]() 3NO2(g)的△H= kJ·mol-1。
3NO2(g)的△H= kJ·mol-1。
(2) T℃时,将0.6 mol NO和0.2 molO3气体充入到2L固定容积的恒温密闭容器中,NO的浓度随反应时间的变化如图1所示。
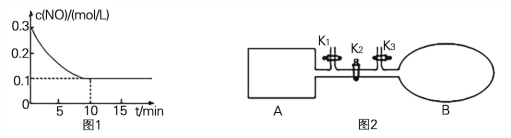
① T℃时,反应3NO(g) +O3 (g) ![]() 3NO2 (g)的平衡常数K= 。
3NO2 (g)的平衡常数K= 。
② 不能说明反应达到平衡状态的是 (填写字母)。
A.气体颜色不再改变 B.气体的平均摩尔质量不再改变
C.气体的密度不再改变 D.单位时间内生成O3和NO2物质的量之比为1∶3
II.NO2的二聚体N2O4是火箭中常用氧化剂。完成下列问题:
(3) 如图2所示,A是由导热材料制成的恒容密闭容器,B是一耐化学腐蚀且易于传热的透明气囊。关闭K2,将各1 molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为aL(忽略导管中的气体体积)。
① 容器A中到达平衡所需时间ts,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率v(NO2)= 。
② 平衡后在A容器中再充入0.5 mol N2O4,则重新到达平衡后,平衡混合气中NO2的体积分数(填“变大”、“变小”或“不变”) 。
③ 在②平衡后,打开K2,重新到达新平衡,B气囊的体积为0.8aL,则在打开K2之前,气囊B的体积为 L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“粗盐提纯”实验中,下列操作正确的是( )
A.过滤时用玻璃棒搅拌漏斗内的液体,以加速过滤
B.蒸发到析出晶体时才需要用玻璃棒搅拌
C.待溶液蒸干后即停止加热
D.当蒸发皿中出现较多量晶体时就应停止加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把aLAl2(SO4)3和(NH4)2SO4的混合溶液分成两等份,其中一份加入bmolBaCl2,恰好使溶液中的SO42-离子完全沉淀;另一份加入足量强碱并加热可得到c molNH3气体,则原溶液中的Al3+离子的浓度(mol/L)为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.水杨酸的结构简式为![]() ,
,
(1)下列关于水杨酸的叙述正确的是_______________。
A.![]() 与
与![]() 互为同系物
互为同系物
B.水杨酸分子中所有原子一定都在同一平面上
C.水杨酸既可以看成是酚类物质,也可以看成是羧酸类物质
(2)将水杨酸与___________________溶液作用,可以生成![]() ;请写出将
;请写出将![]() 转化为
转化为![]() 的化学方程式_______________。
的化学方程式_______________。
Ⅱ.用质谱法分析得知某链烃的相对分子质量为124。用酸性KMnO4溶液氧化,得到两种产物:a.CH3COOH, b.![]()
(3)b的名称为________________。
(4)该烃的分子式为________________;写出该烃可能的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相同物质的量的O2和O3的质量比为_________;所含氧原子的个数比为______________。
(2)2.5 mol Ba(OH)2中含有_________个OH—,2.5 mol Ba(OH)2的质量是____________g。
(3)在标准状况下,1.7 g氨气所占的体积约为__________L,它与标准状况________L硫化氢含有相同数目的氢原子。
(4)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为________________。
(5)同温同压下,SO2与氦气的密度之比为________,若质量相同,两种气体的体积比为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com