
【题目】36.5gHCl溶解在1L水中(水的密度近似为1g/mL所得溶液的密度为ρg/mL,质量分数为w,物质的量浓度为cmol/L,NA表示阿伏加德罗常数,则下列叙述不正确的是( )
A.所得溶液的体积为(36.5+1000)/ρ
B.所得溶液的物质的量浓度为![]()
C.所得溶液的溶解度为S=100w/(1-w)
D.所得溶液的质量分数:w=36.5c/1000ρ
科目:高中化学 来源: 题型:
【题目】可逆反应aA(s)+bB(g)![]() cC(g) +dD(g), 当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,以下正确的是( )
cC(g) +dD(g), 当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,以下正确的是( )
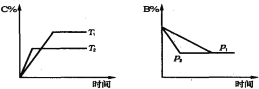
A. T1>T2,正反应放热
B. Tl<T2,正反应吸热
C. P1>P2,a+b>c+d
D. Pl<P2,b=c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,容积为2 L的密闭容器中,将2 mol L气体和3 mol M气体混合,发生如下反应:2L(g)+3M(g)![]() xQ(g)+3R(g),10s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
xQ(g)+3R(g),10s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
(1)10 s末L的物质的量浓度为_____________。
(2)前10 s内用M表示的化学反应速率为_____________。
(3)化学方程式中x值为_____________。
(4)在恒温恒容条件,往容器中加入1 mol氦气,反应速率________(增大、减小、不变)。
(5)在恒温恒压条件,往容器中加入1 mol氦气,反应速率________(增大、减小、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):

请回答下列问题:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是________(填标号)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是________;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是________。
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是___________________。
在分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
A.直接将含碘苯溶液从分液漏斗上口倒出
B.直接将含碘苯溶液从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将含碘苯溶液从下口放出
D.先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体是一种常见的分散系,回答下列问题。
(1)向煮沸的蒸馏水中逐滴加入____________溶液,继续煮沸至__________________,停止加热,可制得Fe(OH)3胶体。
(2)向Fe(OH)3胶体中加入Na2SO4饱和溶液,主要由于________(填离子符号)的作用,使胶体形成了沉淀,这个过程叫作________________。
(3)区分胶体和溶液常用的方法叫作______________,这是因为胶体粒子对光线的________作用而形成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.⑴指出如下图实验装置中的错误之处(加热装置中烧杯底部已垫有石棉网)
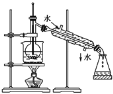
①____________________;
②____________________。
⑵图是某学生的过滤操作示意图,其操作不规范的是______

a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
Ⅱ.海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:Cl2+2KI=2KCl+I2。请回答下列问题:


⑴指出提取碘的过程中有关实验操作①和②的名称:__________;________。
⑵在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象是上图中的_____(注:试管中深色区为有色溶液),上层无色溶液的溶质是_____下层颜色是_____。
⑶从含碘的有机溶液中提取碘和回收有机溶剂,还需经过的操作是_______。
Ⅲ.某溶液中含有MgSO4和Na2SO4两种溶质,选择适当试剂将溶液中的镁离子转化为沉淀或固体分离出来,设计实验流程如下:

欲证明滤液中存在SO42-、OH-,选用的方案是先取少量的滤液滴加________,发现溶液变红,再向其中加入________溶液,出现白色沉淀,则可证明SO42-、OH-,均存在。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电化学原理可同时将SO2、CO2变废为宝,装置如图所示(电极均为惰性电极)。下列说法不正确的是

A. a为负极,发生氧化反应
B. 装置工作时,电子从c极流入b极
C. 若b极消耗16gO2,则Y中左侧溶液质量减轻16g
D. d电极反应式为CO2+6H++6e-=CH3OH+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g)+Y(g) ![]() 2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 反应前2 min的平均速率ν(Z)=2.0×10-3 mol·L-1·min-1
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2 molZ,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的原理及电池中发生的主要反应如图所示。下列说法正确的是

A. 电池工作时,光能转变为电能,X为电池的正极
B. 镀铂导电玻璃的作用是传递I-
C. 电解质溶液中发生反应:2Ru3++3I-=2Ru2++I3-
D. 电池的电解质溶液中I-和I3-的浓度均不断减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com