
 钠、铁和铝是三种重要的金属.请回答:
钠、铁和铝是三种重要的金属.请回答:分析 (1)利用金属活动性顺序表,结合其排在前面的金属的活动性大于后面的金属的意义判断金属活动性强弱;
(2)钠和水反应生成氢氧化钠和氢气;酚酞遇碱变红;
(3)铁和氢氧化钠不反应,铝能和强酸、强碱反应,金属铝与氢氧化钠溶液反应生成了偏铝酸钠和氢气;
(4)FeCl3和NaOH反应生成红褐色沉淀Fe(OH)3;AlCl3中加入NaOH先生成Al(OH)3,Al(OH)3具有两性,可与NaOH反应生成NaAlO2,以此解答.
解答 解:(1)金属活动性顺序是:K、Ca、Na、Mg、Al、Mn、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au,结合活动性前大于后;则钠、铁和铝三种金属活动性由强到弱的顺序是Na、Al、Fe,
故答案为:Na>Al>Fe;
(2)钠是一种非常活泼的金属,将其投入水中,会浮在水面上与水发生剧烈反应,放出的热使其熔化成银白色小球,甚至使生成的氢气燃烧,发生反应的化学方程式为:2Na+2H2O═2NaOH+H2↑,酚酞遇碱变红,③中加入酚酞试液后观察到的现象是溶液变红色,
故答案为:2Na+2H2O═2NaOH+H2↑;溶液变红色;
(3)铝和强酸、强碱反应生成可溶性盐和氢气;铝与氢氧化钠溶液反应,反应生成偏铝酸钠和氢气,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:Al(或铝);2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(4)FeCl3和NaOH反应生成红褐色沉淀Fe(OH)3,化学方程式为FeCl3+3NaOH=Fe(OH)3↓+3NaCl,离子方程式为 Fe3++3OH-=Fe(OH)3↓,AlCl3中加入NaOH先生成白色沉淀Al(OH)3,发生Al3++3OH-═Al(OH)3↓,Al(OH)3具有两性,继续加入NaOH溶液则发生Al(OH)3+OH-═AlO2-+2H2O,可观察到沉淀溶解,
故答案为:Fe3++3OH-=Fe(OH)3↓;b.
点评 本题考查金属活动性的比较、钠与水的反应、铝的化合物的性质等知识,注意金属性的比较,需明确常见的金属性比较的方法,掌握AlCl3中加入NaOH的反应原理是解答的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 | |
| B. | 0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 | |
| C. | 0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 | |
| D. | 1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用铝热剂的反应,常用于冶炼高熔点的金属 | |
| B. | 氧化铝和铁的混合物是铝热剂 | |
| C. | 铝热剂发生的铝热反应需要用镁带和氯酸钾引燃,所以铝热反应是吸热反应 | |
| D. | 工业上常用铝热反应来大量冶炼金属铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不可以用铜丝搅拌棒代替环形玻璃搅拌棒 | |
| B. | 用稍过量的NaOH溶液保证盐酸完全被中和 | |
| C. | 使用环形玻璃搅拌棒是为了加快反应速率,减小实验误差 | |
| D. | 用0.5 mol•L-1NaOH溶液分别与0.5 mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
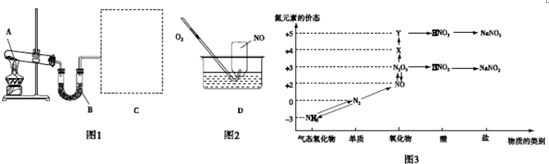
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③⑤ | C. | ③⑤ | D. | 只有① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com