
(2013梅州质检,22)某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表—种元素,其中O点代表氢元素。下列说法中不正确的是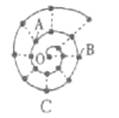
A.离0点越远的元素原子半径越大
B.虚线相连的元素处于同一族
C.B、C最高价氧化物的水化物可相互反应
D.A、B组成的化合物中不可能含有共价键
BC
解析试题分析:依题意,图中A、B、C分别是氧、钠、铝。短周期主族元素中钠元素的原子半径最大,离0点最远的氯元素原子半径比钠小,故A错误;虚线相连的元素处于同一族,如氢、锂、钠,氦、氖、氩等,故B正确;B、C分别是钠、铝,它们的最高价氧化物的水化物分别是氢氧化钠、氢氧化铝,前者是强碱,后者是两性氢氧化物,因此二者能相互反应,即NaOH+Al(OH)3=NaAlO2+2H2O,故C正确;A、B分别是氧、钠,二者可形成的氧化物可能是氧化钠、过氧化钠,Na2O中只含离子键,不含共价键,Na2O2中不仅含离子键,还有共价键,故D错误。
考点:考查物质结构与元素周期律,涉及元素在周期表中的位置、原子结构、元素及其化合物的性质之间的推断等。


科目:高中化学 来源: 题型:单选题
有X、Y、Z、M四种短周期元素,其中X、Y、Z同周期。Z、M同主族,X2+与M2-具有相同的电子层结构;Y的单质常用做电脑的芯片材料。下列说法中正确的是
| A.元素Y的最高价氧化物属于两性氧化物 |
| B.元素M的某种单质可作水处理的消毒剂 |
| C.X、M两种元素形成的化合物中只可能含离子键 |
| D.Y、Z、M三种元素的气态氢化物的热稳定性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲、乙、丙、丁四种短周期主族元素,它们的价电子数依次增大,乙形成的化合物种类最多,甲与乙的原子序数之和等于丁的原子序数,丙和乙位于同一周期,丁和乙位于不同周期。则下列说法中正确的是
| A.甲、乙、丙形成的化合物既有离子键又有共价键 |
| B.乙、丙、丁形成的氢化物常温下均为气体 |
| C.原子序数由小到大顺序为:甲<乙<丙<丁 |
| D.原子半径大小顺序为:丁>甲>乙>丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Q、W、X、Y、Z都是短周期元素。X、Y、Q在周期表中的位置关系如图。W、Z的最外层电子数相同,Z的核电荷数是W的2倍。则下列说法不正确的是
| IA | IIA | IIIA | IVA |
| | | | Q |
| X | | Y | |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A. 14C与12C互为同素异形体 |
| B.高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |
| C.NOx、CO2、PM2.5颗粒都会导致酸雨 |
| D.避免船体遭受腐蚀,在船舶的外壳装上若干锌块,称为外加电流的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是电子层数的三倍,Y与X可形成Y2X2和Y2X两种离子化合物,Z原子的核外电子数比Y原子多1,W与X同主族,则
| A.原子半径:Y< Z < W |
| B.单质的还原性:Y> Z |
| C.气态氢化物的稳定性:X>W |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、R在周期表中的位置如图。下列说法正确的是
| | | ||||
| | | X | Y | | |
| | | | Z | R | |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知a、b分别为同周期的ⅡA族和ⅦA族的两种元素,它们的原子序数分别为m和n,则下列关系不可能成立的是( )
| A.m=" n" —15 | B.n=m+12 | C.m=n —29 | D.n=m+5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍。下列说法正确的是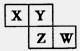
| A.X、Y、Z的原子半径大小:X>Y>Z |
| B.X、W的气态氢化物能相互反应,生成共价化合物 |
| C.Z、W的最高价氧化物对应水化物的酸性,前者更强 |
| D.Y的单质与氢气反应较Z剧烈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com