
下列叙述正确的是 ( )
A.元素的原子序数越大,其族序数也越大
B.同周期的第ⅡA族与第ⅢA族的原子序数一定相差1
C.在元素周期表中,第14列元素所形成的化合物种类最多
D.元素的最外层电子数为奇数,其族序数不一定为奇数
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
化学与环境、生活、材料密切相关。下列说法正确的是( )
A.安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率
B.二氧化氯和三氯化铁都常用于自来水的处理,二者的作用原理是相同的
C.通过有机合成,可以制造出比钢铁更强韧的新型材料
D.气溶胶和液溶胶的差别在于分散质的物质状态
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D为为中学常见单质。通常状况下,A为固体,B为黄绿色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间转化关系如下图所示(其中某些反应条件和部分反应物已略去)。
请回答下列问题:
写出下列物质的化学式:A______、X______。
在反应;① ~⑦中,属于氧化还原反应的有____个;反应⑥说明D溶液中含有___离子。
反应④的离子方程式是__________。
反应⑦的化学方程式是__________。
检验D的溶液中是否含有G离子的方法是_________。
除去D溶液中混有的少量G的方法是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s)+O2(g)====CO2(g) ΔH1<0
途径Ⅱ 先制水煤气:
C(s)+H2O(g)====CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
2CO(g)+O2(g)====2CO2(g) ΔH3<0
2H2(g)+O2(g)====2H2O(g) ΔH4<0
请回答下列问题:
(1)判断两种途径放热:途径Ⅰ放出的热量______途径Ⅱ放出的热量(填“大于”“等于”或“小于”)。
(2)ΔH1、ΔH2、ΔH3、ΔH4的数学关系是________________________。
(3)由于制取水煤气的反应里,反应物具有的总能量_______(填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要_______能量才能转化为生成物,因此其反应条件为_________________。
(4)已知:Fe2O3(s)+3CO(g)====2Fe(s)+3CO2(g)
ΔH1=-25 kJ·mol-1①
3Fe2O3(s)+CO(g)====2Fe3O4(s)+CO2(g)
ΔH2=-47 kJ·mol-1②
Fe3O4(s)+CO(g)====3FeO(s)+CO2(g)
ΔH3=+19 kJ·mol-1③
请写出CO还原FeO的热化学方程式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如表所示为元素周期表的一部分,参照元素①~⑦在表中的位置,请回答下列问题:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(1)③、④、⑦的原子半径由大到小的顺序为 (用元素符号表示)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为 (用酸的化学式表示)。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式 ;
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
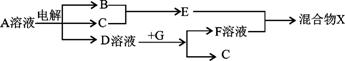
①写出D溶液与G反应的化学方程式 。
②写出检验A溶液中溶质的阴离子的方法 。
③常温下,若电解1L0.1 mol·L-1的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为 。
④写出过量的E与F溶液中溶质反应的离子方程式 。
(5)由②、④、⑥元素组成的化合物W(在酸性溶液中发黄,W还原性较强),在溶液中易被⑦的单质氧化,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表回答问题:
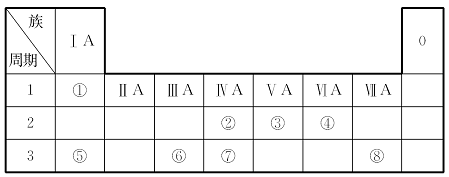
(1)元素⑦在周期表中的位置是___________________。
(2)元素①和⑤的原子序数相差 。
(3)写出元素⑤形成的常见化合物与元素⑧形成的单质反应的化学方程式____
__________________________。
(4)写出元素③形成的不同化合价的化合物的化学式(写出四个)____________
___________________________________________________________________,
其中能与元素⑥形成的单质反应的化学方程式为_________________________
__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.化学反应中的能量变化,都表示为热量的变化
B.需要加热才能发生的化学反应,一定是吸热反应
C.放热反应在常温下一定很容易发生
D.反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小
查看答案和解析>>
科目:高中化学 来源: 题型:
已知298 K时,合成氨反应N2(g)+3H2(g)===2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失)( )
A.一定小于92.0 Kj B.一定大于92.0 kJ
C.一定等于92.0 kJ D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
共价键、离子键和分子间作用力是微粒之间的三种作用力。下列晶体①Ba(OH)2 ②SiO2 ③石墨 ④KCl ⑤干冰中,含有两种作用力的是( )
A.①②③ B.①③⑤
C.②④⑤ D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com