
| A. | 200ml 2mol/L Mg Cl2溶液 | B. | 1000 ml 2.5 mol/LNaCl | ||
| C. | 300 ml 5 mol/L K Cl 溶液 | D. | 250 ml 1 mol/L AlCl3 |
分析 溶液中c(Cl-)=溶质的物质的量浓度×化学式中氯离子个数计算,注意氯离子浓度与溶质的组成及溶液的浓度有关,与溶液的体积的大小无关.
解答 解:A.2mol/L MgCl2溶液中,氯离子的浓度为:2×2mol/L=4mol/L;
B. 2.5mol/L 氯化钠溶液中,氯离子的浓度为:1×2.5mol/L=2.5mol/L;
C.5mol/L KCl溶液,氯离子浓度为:1×5mol/L=5mol/L;
D.1mol/L AlCl3溶液中,氯离子的浓度为:3×1mol/L=3mol/L;
所以溶液中Cl-物质的量浓度最小的是2.5mol/L,
故选:B.
点评 本题考查学生对物质的量浓度的理解,难度不大,注意溶液中溶质离子的浓度与溶质的组成及溶液的浓度有关,与溶液体积无关.


科目:高中化学 来源: 题型:解答题
 阿司匹林可由水杨酸与乙酸酐作用制得.其制备原理如下:
阿司匹林可由水杨酸与乙酸酐作用制得.其制备原理如下: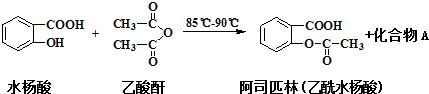

 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2OH | B. | CH3OCH3 | C. | CH2=CH-CH3 | D. | 一氯苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32克 O2与O3所含的原子数目相同,均为NA | |
| B. | 46克的NO2和N2O4混合气体中含原子数目为3 NA | |
| C. | 18克的NH4+中含有电子数为NA | |
| D. | 28 g Fe变为离子时,失去的电子数一定为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X:AlCl3、Mg(NO3)2、HNO3;Y:NaOH | |
| B. | X:Na2CO3、NH4HCO3、Na2SO4;Y:Ba(OH)2 | |
| C. | X:NH4NO3、Al(NO3)3、Fe(NO3)3、HCl;Y:NaOH | |
| D. | X:NaAlO2、氨水、NaOH;Y:H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(s,单斜)═S(s,正交)△H=+0.33kJ•mol?1,正交硫比单斜硫稳定 | |
| B. | 2H2(g)+O2(g)═2H2O(g);△H=-489.6kJ•mol-1,氢气的燃烧热为489.6kJ•mol-1 | |
| C. | 当镀锌铁制品的镀层破损时,镀层仍能对铁制品起到保护作用 | |
| D. | 锌锰干电池工作一段时间后碳棒变细 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | α1=α2 | B. | a+b=14 | C. | a<b | D. | a<7,b>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com