
【题目】用铂电极电解CuSO4和Al2(SO4)3的混合液一段时间后,往溶液中加入0.5mol Cu2(OH)2 CO3恰好使溶液复原,则电解过程转移的电子的物质的量为( )
A.1 molB.2 molC.3 molD.4 mol
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中进行化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________。
(2)该反应为____________(填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____________℃。
(4)在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2 mol·L-1,c(H2)=1.5 mol·L-1,c(CO)=1 mol·L-1,c(H2O)=3 mol·L-1,则下一时刻,反应____________(填“正向”或“逆向”)进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应:Zn+2H+=H2↑+Zn2+,设计如图所示原电池,观察到Y电极上有气泡产生,下列说法错误的是( )
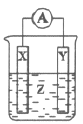
A.Y电极可能是铜
B.Z可能是硫酸铜溶液
C.电子流动方向:X→导线→Y
D.X电极的反应式:Zn-2e-=Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一绝热容积不变的密闭容器中发生可逆反应![]() ,以下不能说明该反应达到化学平衡状态的是( )
,以下不能说明该反应达到化学平衡状态的是( )
A.混合气体的密度不再变化B.v逆(X)=v正(Y)
C.X、Y的浓度比为1:1D.体系压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年春节前后,世界各地爆发了新型冠状病毒疫情。在疫情面前,我国人民众志成城,奋力战疫。
(1)疫情期间,更应合理饮食。山西人喜欢以“面”为主食,“面”中富含的营养物质是___,面在人体中各种酶的作用下发生水解,最终生成___(填化学式),与其互为同分异构体的一种物质的名称是___。
(2)加强锻炼,增强体质,是抗疫的最佳途径。通过锻炼可以消耗身体内多余脂肪,脂肪在人体中所起的主要作用是___。
(3)医用口罩中对阻挡病毒起关键作用的是熔喷布(主要原料是聚丙烯),由丙烯(CH3CH=CH2)在一定条件下制取聚丙烯的化学方程式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,若开始时a、b两端液面相平,放置一段时间后,下列有关叙述中正确的是( )
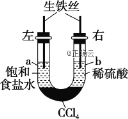
A.铁丝在两处的腐蚀速率:a>b
B.a、b两端相同的电极反应式为![]()
C.一段时间后,a端液面高于b端液面
D.a处总反应为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中常含有的NOx、SO2、H2S等污染物,容易形成酸雨,破坏环境。其综合治理是当前重要的研究课题。
Ⅰ.以下是对酸雨的若干项评价,其中不正确的是__________
a.杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.导致臭氧层空洞
d.二氧化碳的过量排放,是形成酸雨的主要原因之一
Ⅱ.电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。

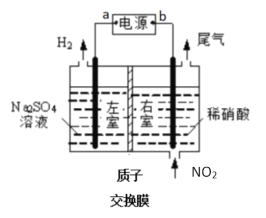
(1)电解NO制备NH4NO3原理如上方左图所示:
①阳极为石墨_____(填1或2),该电极的反应式为_____________。
②为使电解的副产物也完全转化为NH4NO3,需要补充的物质X的化学式为___________。
(2)用上方右图装置进行模拟电解NO2气体实验,可回收硝酸。
①外接电源a极为______极,左室发生的电极反应式为_____________。
②若有标准状况下2.24L NO2被吸收,通过质子交换膜(只允许质子通过)的H+为______mol。
③用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中增加了1 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28L H2。原气体中NO和NO2的体积比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是

A. 该分子中含有1个手性碳原子
B. 1mol乙酰紫草素最多可与2mol NaOH反应
C. 1mol 乙酰紫草素最多可与2mol Br2反应
D. 能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业的重要反应之一:2SO2(g)+O2(g)![]() 2SO3(g)下列叙述不正确的是( )
2SO3(g)下列叙述不正确的是( )
A.其他条件不变,升高温度可增大SO3的生成速率
B.使用合适的催化剂,是为了增大化学反应速率
C.该反应达到化学平衡状态时,SO2可100%转化为SO3
D.该反应达到化学平衡状态时,SO3的浓度不再改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com