
【题目】根据你对金属钠性质的了解,回答下列问题:
(1)关于钠的叙述中,正确的是________(填字母)。
A.钠是银白色金属,硬度很大
B.将金属钠放在石棉网上,用酒精灯加热后金属钠剧烈燃烧,产生黄色火焰,生成过氧化钠
C.金属钠在空气中燃烧,生成氧化钠
D.金属钠的熔点很高
(2)由于金属钠很容易跟空气中的______、________等物质反应,通常将它保存在_______里。
(3)将一小块钠投入到下列溶液中,既能产生气体又会出现白色沉淀的是________(填字母)。
A.稀硫酸 B.硫酸铜溶液
C.氢氧化钠溶液 D.氯化镁溶液
(4)为粗略测定金属钠的相对原子质量,设计的装置如图所示,该装置(包括水)的总质量为ag,将质量为bg的钠(不足量)放入水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为cg。

①列出计算钠相对原子质量的数学表达式______________(用含有a、b、c的算式表示)。
②无水氯化钙的作用是____________________。
【答案】B 氧气 水蒸气 煤油 D b/(a+b-c) 吸收H2中所含的H2O(g)
【解析】
(1)根据钠的性质分析解答;
(2)钠的性质很活泼,易和水、氧气反应,据此解答;
(3)金属钠投入水中生成氢氧化钠和氢气,根据溶液中的溶质分析解答;
(4)①根据钠与水反应产生氢气的质量关系以及反应前后质量差解答;
②根据产生的气体中含有水蒸气分析判断。
(1)A、钠是银白色金属,硬度很小,可以用小刀切,故A错误;
B、钠在空气中燃烧产物是淡黄色的过氧化钠,故B正确;
C、钠在空气中燃烧产物是淡黄色的过氧化钠,不是氧化钠,故C错误;
D、金属钠的熔点很低,故D错误;
故答案选B;
(2)钠性质很活泼,易和水、氧气反应,所以保存钠时要隔绝空气和水,钠和煤油不反应,且密度大于煤油,所以保存钠可以放在煤油中;
(3)A.钠和稀硫酸反应生成硫酸钠和氢气,没有沉淀产生,A不选;
B.钠投入硫酸铜溶液中,首先和水反应生成氢氧化钠和氢气,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,但沉淀不是白色的,而是蓝色的,B不选;
C.钠投入氢氧化钠溶液中生成氢氧化钠和氢气,没有沉淀,C不选;
D.钠投入氯化镁溶液中生成氯化钠、氢氧化镁白色沉淀和氢气,D选。
答案选D。
(4)①金属与水发生反应放出氢气的质量=ag+bg-cg=(a+b-c)g,假设金属为R,其相对原子质量为M,根据金属钠与水反应放出氢气的关系,可推断该金属与水放出氢气关系如下:
2R~~~~~H2
2M 2
bg (a+b-c)g
解得M=b/(a+b-c);
②氯化钙具有吸水能力,是常用的干燥剂,在装置中吸收生成氢气中的水,而防止水分流失。


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种工业盐,在生产、生活中应用广泛,外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,但使用过量会使人中毒。某学习小组通过如下装置(夹持及加热装置略去)制取NaNO2样品并对样品含量进行测定
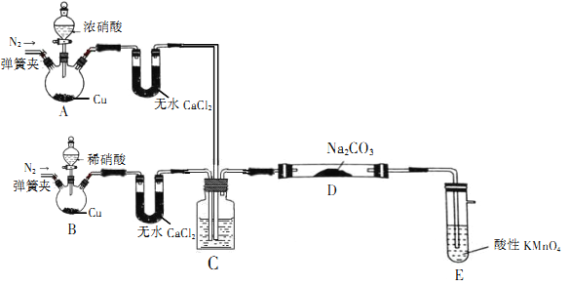
该小组先查阅资料知:NO、NO2能被酸性高锰酸钾氧化为NO3-。
(1)装置A中用于盛放浓硝酸的仪器名称为__________,装置D中发生的化学反应方程式为___________。
(2)①装置C中所装的液体需满足的条件是____________________。
②其作用为____________________。
(3)装置E的作用是____________________。
(4)为测定制得样品中NaNO2的含量,该实验中需配制KMnO4标准溶液并酸化,应选择__________(填化学式)来酸化KMnO4溶液。
(5)已知:在酸性溶液中,NO2-可将MnO4-还原为Mn2+。为测定样品中亚硝酸钠的含量,该小组称取4.0g样品溶于水配制成250mL溶液,取25.00mL溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液进行滴定,消耗20.00mL酸性KMnO4溶液(杂质不反应)。滴定过程中酸性KMnO4溶液的作用是____________________,所得样品中NaNO2的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中粒子的物质的量浓度关系正确的是( )
A. 0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO![]() )>c(HCO
)>c(HCO![]() )>c(OH-)
)>c(OH-)
B. 20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C. 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH![]() )+c(OH-)
)+c(OH-)
D. 0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中: c(OH-)>c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了清理路面积雪,人们常使用一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54mol电子。
(1)该融雪剂的化学式是____,该物质中化学键类型是______,电子式是______。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是__________;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e-稳定结构,该分子的结构式为_________,电子式为_______,化学键类型为_________(填“离子键”“非极性共价键”或“极性共价键”)。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:不加热时生成____,其化学键类型为___;加热时生成_____,其化学键类型为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NaHCO3的NaCl。某学生设计了如图所示方案提取纯净的NaCl溶液。

如果此方案正确,那么:
(1)操作④为________,操作①、④、⑤都用到的玻璃仪器有____________。
(2)操作②为什么不用硝酸钡溶液,其理由是___________________________________。
(3)进行操作②后,如何判断SO42-已除尽,方法是_______________________________。
(4)操作③的目的是____________,为什么不先过滤后加碳酸钠溶液?理由是____________。
(5)操作⑤的目的是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将过量的0.2g铜粉与5mL1 molL1FeCl3溶液混合,充分振荡,溶液棕黄色变浅,溶液变绿,有灰白色固体出现。通过查阅资料,初步认为灰白色固体可能含CuCl(CuCl白色晶体,不溶于水、硫酸、稀硝酸,溶于氨水、浓盐酸溶液中,生成络合物)。为进一步探究灰白色固体是否含CuCl,进行一系列实验。已知:① CuCl+2NH3H2O![]() [Cu(NH3)2]++Cl+2H2O(无色溶液)② 提供的试剂:稀HNO3、AgNO3溶液、氨水、KSCN溶液
[Cu(NH3)2]++Cl+2H2O(无色溶液)② 提供的试剂:稀HNO3、AgNO3溶液、氨水、KSCN溶液
请回答下列问题:
(1)生成CuCl的化学方程式____________________________________。
(2)下列为常见的分离装置(装置中的其他仪器忽略),从上述溶液中分离出固体混合物,应选用的相应装置中的仪器名称是_______________。
A. B.
B.  C.
C.![]() D.
D. E.
E. F.
F.
(3)提纯灰白色固体:将固体混合物用蒸馏水洗涤以除去固体表面的Fe3+、Cl。为检验固体混合物是否洗涤干净,最佳方案是检验洗涤液中是否含有_______(填离子符号),理由是_____________________________________________。
(4)设计实验检验得到的灰白色固体中含有CuCl,该实验过程中用到的试剂为____________________。
(5)实验测得灰白色固体混合物质量为a g,其中CuCl b g。上述实验过程中还有CuCl2生成,则生成CuCl2的物质的量是____________(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H为某合成药物的中间体,其合成路线如下:

已知:
① R-CH=CH-CH3 ![]() R-CH=CH-CH2-Br
R-CH=CH-CH2-Br
② RCH=CH2+HBr![]() RCH2CH2Br
RCH2CH2Br
回答下列问题:
(1)A的结构简式为_______。H中含有的含氧官能团名称是__________。
(2)F→G的反应类型为__________,设计C→D的目的为___________。
(3)D→E反应的化学方程式为_____________________________。
(4)M和N与G互为同分异构体。M含有苯环,苯环上有2个支链,且苯环上一氯代物只有2种,遇FeCl3溶液显紫色,能与新制Cu(OH)2悬浊液反应生成砖红色沉淀,则M有_____种(不考虑顺反异构)。N为芳香族化合物,0.5molN与足量银氨溶液反应生成2molAg,核磁共振氢谱显示其峰面积比为1:2:2,则N的结构简式为________。
(5)参考上述合成路线,以丙烯为原料(无机试剂任选)设计制备![]() 的合成路线____________________。
的合成路线____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,四种均为0.1molL﹣1的溶液,其pH如下表所示:
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaHCO3 |
|
pH | 7.0 | 7.0 | 8.4 | 9.9 |
下列关系不正确的是
A. 酸性:H2CO3 > ![]()
B. 水电离产生的c(H+):① = ②
C. 溶液③中:c(HCO3﹣)+ c(CO32﹣)+ c(H2CO3)= 0.1molL﹣1
D. 溶液④中:c(Na+)> c(![]() )> c(OH-)> c(H+)
)> c(OH-)> c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com