
| A. | Na+、Ag+、NO3-、Br- | B. | Cu2+、SO42-、Cl-、H+ | ||
| C. | Na+、Mg2+、SO42-、Cl- | D. | Ca2+、K+、OH-、CO32- |
分析 无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.银离子与溴离子反应生成溴化银沉淀;
B.铜离子为有色离子,不满足溶液无色的条件;
C.四种离子之间不反应,都是无色离子;
D.钙离子与碳酸根离子反应生成碳酸钙沉淀.
解答 解:无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.Ag+、Br-之间反应生成难溶物溴化银,在溶液中不能大量共存,故A错误;
B.Cu2+为有色离子,不满足溶液无色的要求,故B错误;
C.Na+、Mg2+、SO42-、Cl-之间不发生反应,都是无色离子,在溶液中能够大量共存,故C正确;
D.Ca2+、CO32-之间反应生成难溶物碳酸钙,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 分离方法 | 原理 |
| A | 除去CO2中的HCl | 通入饱和Na2CO3溶液 | HCl和Na2CO3溶液反应生成CO2 |
| B | 除去乙醇中少量的乙酸 | 加入足量生石灰蒸馏 | 乙醇和乙酸钙的沸点相差较大 |
| C | 除去KNO3固体中NaCl | 冷却热饱和溶液重结晶 | NaCl在水中的溶解度很大 |
| D | 分离乙酸和乙醇 | 用分液漏斗分液 | 乙醇乙酯和乙醇的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浅黄色固体 | B. | 应密封保存 | ||
| C. | 与CO2反应时,CO2作还原剂 | D. | 与H2O反应时,放出大量的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2和O3互为同位素 | B. | 1个15O2中含有18个中子 | ||
| C. | 18O2与16O2的性质完全相同 | D. | 16O和18O的核外电子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
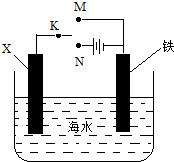
| A. | 若X为碳棒,为减缓铁的腐蚀,开关K应置于N处 | |
| B. | 若X为碳棒,开关K置于M处,会加快铁的腐蚀 | |
| C. | 若X为锌,开关K置于M处,就是牺牲阳极的阴极保护法 | |
| D. | 若X为锌,开关K置于N处,铁电极发生的反应为Fe-2e-═Fe${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
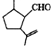 ,下列说法正确的是( )
,下列说法正确的是( )| A. | M的分子式为C10H14O | |
| B. | M能发生氧化反应,不能发生还原反应 | |
| C. | M与FeCl3溶液反应生成紫色有机化合物 | |
| D. | 检验M中官能团是先加入新制氢氧化铜,微热,酸化后再加溴水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com