
| AgNO3 | Ba(NO3)2 | AgCl | BaCl2 |
H2O(l) | 1.5×10 | |||
NH3(l) |
(1)上述四种物质在水中发生的复分解反应为________________________。
(2)能在液氨中发生的复分解反应为________________________________。?
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:022
现有K、Y、Z三种元素,已知有如下情况:
(1)X、Y、Z的单在常温下均为气体.
(2)X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰为苍白色.
(3)XZ极易溶于水,在水溶液中电离出 和
和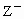 .XZ的水溶可使石蕊试液变红.
.XZ的水溶可使石蕊试液变红.
(4)两分子X的单质可与一分子Y的单质化合,生成两分子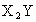 ,
, 常温下为液体.
常温下为液体.
(5)Z的单质溶于 中,所得溶液具有漂白用.
中,所得溶液具有漂白用.
试推断X、Y、Z的元素种类及XZ和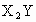 各是何物质,用元素符合和化学式表示:
各是何物质,用元素符合和化学式表示:
X________,Y_________,Z_________,XZ_________,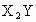 _________.
_________.
查看答案和解析>>
科目:高中化学 来源:黑龙江省哈三中2009-2010学年高一上学期期末考试化学试题 题型:022
如图转化关系中A-H为中学常见化合物,甲、乙、丙、丁为常见单质,其中甲、丁常温为气体.已知单质乙、化合物A为黄色(或淡黄色)固体.乙经过连续与甲反应后,再与水化合,是工业上制H的反应过程.B、F两种气体都能使澄清石灰水变浑浊.(部分反应物或产物略去)

(1)写出下列物质的化学式:A________ F________ 甲________ 丙________
(2)写出下列反应的化学方程式:A与B________ Cu与H________
(3)写出丙与D溶液反应的离子方程式________
(4)常温时H的浓溶液与丙物质并不能看到明显的反应现象,原因是________.
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:2012-2013学年云南省德宏州潞西市芒市中学高二(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2012-2013学年云南省德宏州潞西市芒市一中高二(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com