
| A. | 在含有NA 个CH3COO-的醋酸溶液中,H+数目略大于NA | |
| B. | 常温下,5.6 L NO和5.6 L O2的混合气体中含有的分子数为0.5NA | |
| C. | 16.9 g BaO2固体中阴、阳离子总数为0.3NA | |
| D. | 含有1 mol Fe(OH)3的氢氧化铁胶体中含有胶粒数为NA |
分析 A.醋酸电离出氢离子和醋酸根离子,根据醋酸溶液中的电荷守恒判断;
B.不是标准状况下,不能使用标准状况下的气体摩尔体积计算;
C.BaO2中的阴离子为O22-,根据n=$\frac{m}{M}$计算出BaO2的物质的量,再计算出含有的阴阳离子数目;
D.氢氧化铁胶粒为氢氧化铁的聚集体.
解答 解:A.在含有NA 个CH3COO-的醋酸溶液中,根据电荷守恒c(H+)=c(CH3COO-)+c(OH-)可知H+数目略大于NA,故A正确;
B.常温下,不是标准状况下,不能使用标准状况下的气体摩尔体积计算气体的物质的量,故B错误;
C.16.9gBaO2的物质的量为$\frac{16.9g}{169g/mol}$=0.1mol,0.1molBaO2中含有0.1mol钡离子和O22-,总共含有0.2mol阴阳离子,则含有的阴、阳离子总数为0.2NA,故C错误;
D.由于氢氧化铁胶粒为氢氧化铁的聚集体,则1 mol Fe(OH)3的氢氧化铁胶体中含有胶粒数小于NA,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标准状况下气体摩尔体积的使用条件,试题培养了学生的灵活应用能力.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.同温同压下,物质的物质的量相等,其体积一定相同
B.等体积的二氧化碳和一氧化碳所含的分子数一定相等
C.1L氮气一定比1L氧气的质量小
D.相同条件下的一氧化碳气体和氮气,若体积相等,则质量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4 | B. | NaOH | C. | Na2SO4 | D. | NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠加入到CuSO4溶液中:2Na+Cu2+═Cu+2Na+ | |
| B. | 铁粉加入到FeCl3溶液中:Fe+2Fe3+═3Fe2+ | |
| C. | 金属铝加入到NaOH溶液中:Al+2OH-+H2O═AlO2-+2H2↑ | |
| D. | 铜片插入到AgNO3溶液中:Cu+Ag+═Cu2++Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 煤、天然气、石油综合利用是构建节约型、环境友好型社会的必然选择.
煤、天然气、石油综合利用是构建节约型、环境友好型社会的必然选择.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LH2O所含分子数为0.5NA | |
| B. | 1mol•L-1CaCl2溶液中所含Ca2+离子的数目为NA | |
| C. | 通常状况下,32gO2与32gO3所含的氧原子数均为2NA | |
| D. | 0.1molZn与含0.1molHCl的盐酸溶液充分反应,转移电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
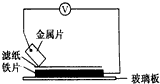 将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表如示说法正确的是D
将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表如示说法正确的是D| A.在四种金属中C的还原性最弱 |
| B.金属B能从硫酸铜溶液中置换出铜 |
| C.AD若形成原电池时A为正极 |
| D.AB形成合金时,将该合金露置在空气中,A先被腐蚀 |
| 金属 | 电子流动方向 | 电压/V |
| A | A→Cu | +0.78 |
| B | Cu→B | +0.15 |
| C | C→Cu | +1.35 |
| D | D→Cu | +0.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氯碱工业中电解饱和食盐水的原理示意图如图所示:
氯碱工业中电解饱和食盐水的原理示意图如图所示:查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:填空题
用Cl2生产某些含氯有机物时会产生副产物HC1。利用 反应A,可实现氯的循环利用。
反应A,可实现氯的循环利用。
反应A:4HCl+O22Cl2+2H2O
(1)已知:Ⅰ、反应A中, 4mol HCl被氧化,放出115.6kJ的热量。
4mol HCl被氧化,放出115.6kJ的热量。
Ⅱ、
①反应A的热化学方程式是________________________。
②断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为__________kJ,H2O中H—0 键比HCl中H—Cl键(填“强”或“弱”)_______________。
(2)合成氨工厂常通过测定反应前后混合气体的密度来确定氨的转化率。某工厂测得合成塔中N2、H2混合气体的密度为0.5536g/L(标准状况),从合成塔中出来的混合气体在相同条件下密度为0.693g/L(标准状况)。该合成氨厂N2的转化率为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com