
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | 2FeO+Si$\frac{\underline{\;高温\;}}{\;}$2Fe+SiO2 | ||
| C. | SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑ | D. | CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3 |
分析 炼铁时加入的石灰石在高温下分解生成生石灰和二氧化碳,生石灰能够与二氧化硅在反应高温条件下反应生成硅酸钙,起到造渣剂作用除去脉石;反应中生成的二氧化碳能够与碳反应生成还原剂一氧化碳,同时二氧化硅能够与焦炭发生氧化还原反应生成碳化硅和一氧化碳,据此解答.
解答 解:炼铁时加入的石灰石在高温下分解生成生石灰和二氧化碳,化学方程式:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,生成的氧化钙能够二氧化硅在反应高温条件下反应生成硅酸钙,方程式:CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3;分解生成的二氧化碳能够与碳反应生成一氧化碳,方程式:CO2+C$\frac{\underline{\;\;△\;\;}}{\;}$2CO,同时二氧化硅能够与焦炭发生氧化还原反应生成碳化硅和一氧化碳,方程式:SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑,因为该过程中没有单子硅,所以不能发生氧化亚铁与硅的反应,
故选:B.
点评 本题考查了高炉炼铁过程,侧重考查石灰石在高炉炼铁中作用,明确反应原理即可解答,题目难度不大.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol/L的氨水中有0.1NA个NH4+ | |
| B. | 在标准状况下22.4L SO3有4NA个原子 | |
| C. | 标准状况下,22.4LNO与11.2LO2混合后气体的分子数为2NA | |
| D. | 7.8g Na2S和Na2O2的混合物中所含离子数为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
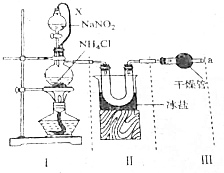 氮气、氨及铵盐用途非常广泛.回答下列问题:
氮气、氨及铵盐用途非常广泛.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 序号 | 金属 质量/g | 金属 状态 | c(H2SO4) mol/L | V(H2SO4) mL | 溶液温度/℃ | 金属消失 的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.7 | 50 | 20 | 35 | 250 |
| 2 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池可将热能直接转变为电能 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 氢氧燃料电池工作时氢气在正极被氧化 | |
| D. | 以KOH溶液为电解质溶液的氢氧燃料电池,正极反应为O2+2H2O+4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
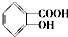 .
.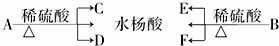
 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com