
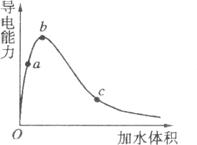
A.a、b、c三点溶液的pH:c<a<b
B.a、b、c三点醋酸的电离程度:a<b<c
C.若用湿润pH试纸测量。点溶液的pH,测量结果会偏小
D.a、b、c三点溶液用1moL/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| 高温 |
| ||
| 高温 |
| 4 |
| 7 |
| ||
| 高温 |
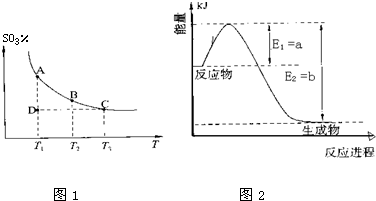
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 催化剂 |
| 高温高压 |
| ||
查看答案和解析>>
科目:高中化学 来源:2011届云南省蒙自高级中学高三1月月考(理综)化学部分 题型:填空题
(1)已知:N2(g)+O2(g)=2NO(g);△H= +180.5kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905kJ/mol
2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol
则N2(g)+3H2(g)=2NH3(g)的△H= 。
(2)工业合成氨的反应为N2(g)+3H2(g)  2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是 。
2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是 。
①增大压强 ②通入He
③使用催化剂 ④降低温度
(3)工业合成氨的反应为N2(g)+3H2(g)  2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为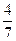 。计算该条件下达到平衡时N2转化率为 ;
。计算该条件下达到平衡时N2转化率为 ;
(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行右图所示实验:(其中c、d均为碳棒,NaCl溶液的体积为500ml)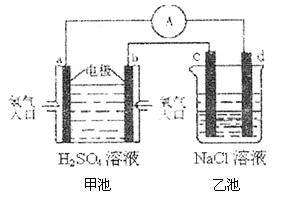
①b极为 极,电极反应式 ;
c极为 极,电极反应式 
②右图装置中,当b极上消耗的O2在标准状况下的体积为280ml时,则乙池溶液的PH为 (假设反应前后溶液体积不变,且NaCl溶液足量)
查看答案和解析>>
科目:高中化学 来源:2010-2011学年云南省高三1月月考(理综)化学部分 题型:填空题
(1)已知:N2(g)+O2(g)=2NO(g);△H= +180.5kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905kJ/mol
2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol
则N2(g)+3H2(g)=2NH3(g)的△H= 。
(2)工业合成氨的反应为N2(g)+3H2(g)
 2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是
。
2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是
。
①增大压强 ②通入He
③使用催化剂 ④降低温度
(3)工业合成氨的反应为N2(g)+3H2(g)
 2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为 。计算该条件下达到平衡时N2转化率为
;
。计算该条件下达到平衡时N2转化率为
;
(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行右图所示实验:(其中c、d均为碳棒,NaCl溶液的体积为500ml)

①b极为 极,电极反应式 ;
c极为 极,电极反应式
②右图装置中,当b极上消耗的O2在标准状况下的体积为280ml时,则乙池溶液的PH为 (假设反应前后溶液体积不变,且NaCl溶液足量)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com