
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
A.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S
B.若X+和Y2-的核外电子层结构相同,则原子序数:X>Y
C.在元素周期表中,硅、锗都位于金属与非金属的交界处,都可以作半导体材料
D.Cs和Ba分别位于第六周期ⅠA族和ⅡA族,碱性:CsOH>Ba(OH)2
科目:高中化学 来源: 题型:
某学生用量筒量取液体,初次视线与量筒内凹液面的最低处保持水平,读数为9.8mL。倒出部分液体后,俯视凹液面的最低处,读数为3.5mL,则该学生实际倒出液体的体积( )
A.大于6.3mL B.小于6.3mL C.等于6.3mL D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式书写正确的是(ΔH的绝对值均正确)( )
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)
ΔH=-1367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l)
ΔH=+57.3 kJ·mol-1(中和热)
C.S(s)+O2(g)===SO2(g) ΔH=-296.8 kJ·mol-1(反应热)
D.2NO2= ==O2+2NO ΔH=+116.2 kJ·mol-1(反应热)
==O2+2NO ΔH=+116.2 kJ·mol-1(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生产、生活、社会密切相关,下列说法正确的是 ( )
A.漂白粉、漂粉精可用来漂白棉、麻、纸张,不能用作游泳池及环境的消毒剂
B.硫酸工业中,从吸收塔上部导出的气体再次通入接触室进行二次氧化,进一步吸收后,二氧化硫的含量很少,可直接排放到空气中
C.工业上可用氯化钠制备化肥NH4Cl
D.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,PM2.5比胶体粒子小,因其比表面积大,故可吸附重金属离子,入肺后对人体产生很大的危害
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质和该性质的应用均正确的是 ( )
A.常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸
B.二氧化硅不与任何酸反应,可用石英制造耐酸容器
C.二氧化氯具有还原性,可用于自来水的杀菌消毒
D.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述与对应图式正确的是 ( )
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 主要化合价 | -2 | +2 | +1 | +5、-3 | +7、-1 | +1 | +5、-3 | +3 |

A.由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强
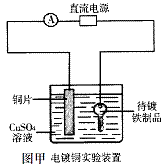
B.图甲装置中,待镀铁制品应与电源负极相连
C.图乙表示H2与O2发生反应过程中的能量变化,则H2的燃烧热的热化学方程式为:
2H2(g)+O2(g)=2H2O(g) △H= — 483.6 kJ/mol
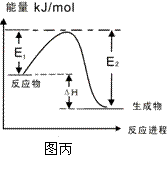
D.图丙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ: CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
② 某温度下,将2mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l) ΔH1=-1451.6kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2 =-566.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(3)某实验小组依据甲醇燃烧的反应原理,
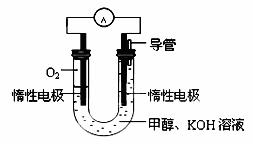 设计如右图所示的电池装置:
设计如右图所示的电池装置:
①该电池的能量转化形式为
。
②工作一段时间后,测得溶液的pH减小。
请写出该电池的负极的电极反应式。
③用该电池电解(惰性电极)500mL某CuSO4溶液,电解一段时间后,为使电解质溶液恢复到原状态,需要向溶液中加入9.8g Cu(OH)2固体。则原CuSO4溶液的物质的量浓度为
mol/L(假设电解前后溶液体积不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室对制备气体反应的基本要求是“反应条件易满足、能平稳地产生气流、所得气体中尽可能不含杂质成分(除少量水蒸气及少量原料汽化形成的物质)”,下列反应一般能用于实验室制备气体的是
A.Na2O2与CO2反应制备O2
B.H2O2与MnO2混合制备O2
C.加热浓硝酸制备NO2
D.浓NaOH与NH4Cl溶液混合加热制备NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学—有机化学基础]3对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
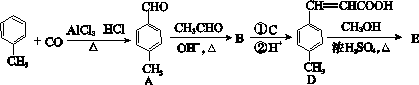
已知:HCHO+CH3CHO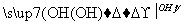 CH2===CHCHO+H2O
CH2===CHCHO+H2O
(1)遇FeCl3溶液显紫色且苯环上有两个取代基的A的同分异构体有____________种,B中含氧官能团的名称为________。
(2)试剂C可选用下列中的________。
a.溴水 b.银氨溶液
c.酸性KMnO4溶液 d.新制Cu(OH)2悬浊液
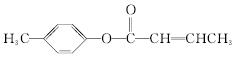 |
(3) 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为____________________。
(4)E在一定条件下可以生成高聚物F,F的结构简式为_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com