
| I |
| KSCN��Һ |
| ������ˮ |
| һ��ʱ��� |
| ʵ���� | ʵ����� | Ԥ������ͽ��� |
| �� | ||
| �� |
| ʵ���� | ʵ����� | Ԥ������ͽ��� |
| �� | ȡ������ɫ�����Һ������KSCN��Һ | ����Һ���ɫ�������2����������Һ�����ɫ�������2������ |
| �� | ȡ������ɫ�����Һ������FeCl3��Һ | ����Һ���ɫ�������1����������Һ�����ɫ�������1������ |


 ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д� ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д� ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ɱ��������Ȼ��� |
| B���ռҺ̬������� |
| C������������������ |
| D��ˮ����ˮ������ˮ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ӳ���Ӧʱ�� |
| B��ʹ�ú��ʵĴ��� |
| C�����ӷ�Ӧ���Ũ�� |
| D���ı䷴Ӧ���¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ˮ��Һ�д���ƽ�⣺
��ˮ��Һ�д���ƽ�⣺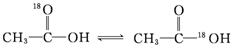 ����ϡ����Ϊ��������
����ϡ����Ϊ��������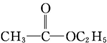 ��H
��H18 2 |
A��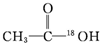 |
B��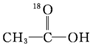 |
| C��C2H5OH |
| D��C2H518OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | ��Cu2+ | ��H+ | ��Cl- | ��SO42- |
| ��c/mol?L-1 | ��0.5 | ��2 | ��2 | ��0.5 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ڢ� | C���ۢ� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 mol CH4�������������г��ȼ�������ȶ����������ȼ����Ϊ-1780.6 kJ?mol-1 |
| B��2 mol CH4�������������г��ȼ������CO2��g����H2O��g����ȼ����Ϊ-890.3 kJ?mol-1 |
| C��1 L 0.1 mol?L-1 NaOH��Һ��1 L 0.1 mol?L-1 HCl��Һ��Ӧ���к���Ϊ-57.3 kJ?mol-1 |
| D��2 L 1 mol?L-1 NaOH��Һ��1 L 1 mol?L-1 H2SO4��Һ��Ӧ�ķ�Ӧ��Ϊ-57.3 kJ?mol-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com