
| A. | 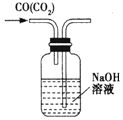 除去CO中的CO2 | B. | 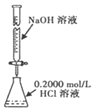 酸碱中和滴定 | ||
| C. | 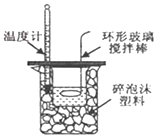 中和热测定 | D. | 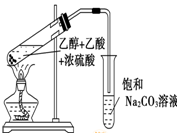 实验室制取乙酸乙酯 |
分析 A.洗气时加入洗气瓶的导管应该“长进短出”;
B.氢氧化钠溶液不能盛放在酸式滴定管中;
C.温度计用于测量酸碱混合液温度,温度计的物质错误;
D.乙醇与乙酸在浓硫酸存在条件下加热制备乙酸乙酯,用饱和碳酸钠溶液吸收乙酸乙酯.
解答 解:A.通过洗气可以除去CO中的CO2,但导管不能短进长出,否则无法洗气,图示装置错误,无法达到实验目的,故A错误;
B.碱式滴定管的下方是橡胶管,图中滴定管是酸式滴定管,不能盛放氢氧化钠溶液,故B错误;
C.中和热的测定中,温度计测量溶液的温度,应该放入酸碱混合液中,图示装置中温度计的位置不合理,故C错误;
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度较小,需要用饱和碳酸钠溶液吸收乙酸乙酯,还需要防止倒吸,图示装置合理,能够达到实验目的,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及物质分离与提纯、中和热测定、乙酸乙酯的制备、中和滴定等知识,明确常见化学实验基本操作方法为解答关键,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | Y与Z位于同一周期 | B. | 单质氧化性:Y<W | ||
| C. | W的氢化物具强还原性 | D. | lmol C中含有离子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①中出现蓝色沉淀 | |
| B. | ③中现象是Cu(OH)2+2OH-?Cu(OH)42-正向移动的结果 | |
| C. | ④中现象证明葡萄糖具有还原性 | |
| D. | 对比②和④可知Cu(OH)2氧化性强于Cu(OH)42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
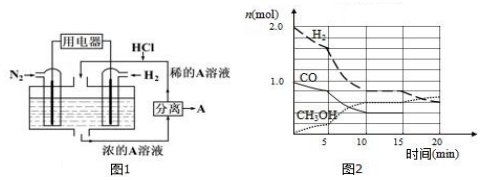
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9.8g由H2SO4和H3PO4组成的混合物中含有的氧原子数为0.4NA | |
| B. | 1mol Na218O2中所含的中子数为42NA | |
| C. | 28g铁粉与足量稀硝酸反应,转移的电子数为NA | |
| D. | 1mol环己烷中含有的共价键数为12NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅熔点高,可用作光导纤维 | |
| B. | 过氧化钠可与二氧化碳反应生成氧气,可用作呼吸供氧剂 | |
| C. | 明矾易溶于水,可用作净水剂 | |
| D. | 二氧化硫有氧化性,可用于漂白纸张 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com