
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在![]() =106mol/L的溶液中Al3+、NH4+、Cl-、SO42-
=106mol/L的溶液中Al3+、NH4+、Cl-、SO42-
B.由水电离的的c(H+)=10-13mol/L溶液中Ca2+、K+、Cl-、HCO3-
C.pH=1的溶液中:Fe2+、Na+、SO42-、NO3-
D.使酚酞呈红色的溶液;Mg2+、ClO-、AlO2-、Na+
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下面有关晶体的叙述中,不正确的是 ( )
A. 氯化铯晶体中,每个Cs+周围紧邻8个Cl-
B. 金刚石为空间网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子
C. 干冰晶体中,每个CO2分子周围紧邻12个CO2分子
D. 金属铜属于六方最密堆积结构,金属镁属于面心立方最密堆积结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《战争的气体化学和分析》中介绍了一种制取COC12(光气,熔点为-118℃,沸点为8.2℃,微溶于水,易溶于甲苯等有机溶剂)的方法,其实验装置如图所示(夹持装置已省略)。已知:3CCl4+2H2SO4(浓) ![]() 3COCl2↑+4HCl+ S2O5Cl2。下列说法正确的是
3COCl2↑+4HCl+ S2O5Cl2。下列说法正确的是

A. 该反应属于氧化还原反应
B. 自来水从冷凝管的X口通入,且被冷凝的物质是CCl4
C. 可将装置丁的尾气通过导管直接通入NaOH溶液中进行尾气处理
D. 装置乙中可收集到光气的甲苯溶液,装置丙、丁均可收集到液态光气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外活动小组为了验证元素化学性质递变规律,进行如下实验探究。
Ⅰ.探究1:验证同周期X、Y、Z三种元素金属性递变规律
实验内容 | 实验现象 |
1、各取1.0g金属X和金属Z,分别加入到5mL水中 | 金属X与水反应比金属Z剧烈 |
2、各取1.0g的金属Z和金属Y(形状相同),分别加入到5mL1.0mol/L盐酸中。 | 金属Z与盐酸反应比金属Y剧烈 |
通过实验验证三种元素金属性由强到弱是_____,则下列判断正确的是(__________)
A.原子序数:Y>Z>X B.原子的最外层电子数X>Y>Z
C.原子半径:Y>Z>X D.Y的最高价氧化物对应水化物的碱性最强
Ⅱ.探究2:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:
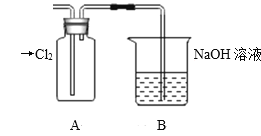
(1)装置A中盛放的试剂是_______(填选项),化学反应方程式是_________。
A.Na2SO3溶液 B.Na2S溶液 C.Na2SO4溶液
(2)下列不能用于验证氯元素比硫元素非金属性强的依据为______(填选项)。
A.HCl比H2S稳定
B.HClO氧化性比H2SO4强
C.HClO4酸性比H2SO4强
D.铁与Cl2反应生成FeCl3,而硫与铁反应生成FeS
(3)若要验证非金属性:Cl>I,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液_______的现象,即可证明。用原子结构理论解释非金属性Cl>I的原因:同主族元素从上到下,________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活生产密切相关。下列说法中错误的是
A.施肥时,铵态氮肥不能与草木灰(含K2CO3)混合使用
B.钡中毒患者可尽快使用苏打溶液洗胃,将Ba2+转化为BaCO3而排出
C.夏天冰箱保鲜食品的原理是降低温度,减慢化学反应速率
D.纯碱溶液显碱性,加热去油污效果更佳。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池与电解池在生活和生产中有着广泛应用。下列有关判断中正确的是
A.装置甲研究的是电解CuCl2溶液,阳极发生的反应:2Cl-+2e-===Cl2↑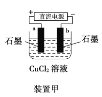
B.装置乙研究的是金属的吸氧腐蚀,Fe上的反应为Fe-3e-===Fe3+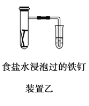
C.装置丙研究的是电解饱和食盐水,B电极发生的反应:2H2O+2e-===H2↑+2OH-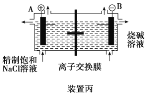
D.向装置丁烧杯a中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成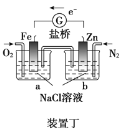
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产中含Cu2+的废水常用MnS(s)作沉淀剂,其反应原理为Cu2+(aq)+MnS(s)![]() CuS(s)+Mn2+(aq)。下列有关该反应的推理错误的是
CuS(s)+Mn2+(aq)。下列有关该反应的推理错误的是
A.该反应达到平衡时:c(Cu2+)=c(Mn2+)
B.相同温度下,CuS的溶解度比MnS的溶解度小
C.向含有等物质的量的CuSO4和MnSO4混合溶液中逐滴加入Na2S溶液,最先出现CuS沉淀
D.往平衡体系中加入少量CuSO4(s)后,c(Mn2+)变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d为短周期主族元素,a的第三电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d属于同周期元素,且d的原子半径小于c的原子半径。下列叙述错误的是( )
A.四种元素中,元素d的非金属性最强
B.元素a、b、c均存在两种或两种以上的氧化物
C.只有元素a与题述其他元素生成的化合物都是离子化合物
D.元素c、d分别与氢元素形成的最简单氢化物中的化学键均为非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积不变的容器中发生2HI(g)H2(g)+I2(g),下列叙述中可以说明反应2HI(g)H2(g)+I2(g)已达到平衡状态的是( )
①单位时间内生成nmolH2的同时生成nmolHI
②反应体系的颜色不再变化
③百分组成w(HI)=w(I2)
④反应速率v(H2)=v(I2)=![]() v(HI)
v(HI)
⑤c(HI):c(H2):c(I2)=2:1:1
⑥v分解(HI)=v生成(HI)
⑦压强不变
A.①③⑤B.②⑥C.④⑤D.④⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com