
| A. | 氯原子:$\underset{\stackrel{••}{Cl}}{••}$• | B. | 硫离子:$\underset{\stackrel{••}{S}}{••}$:2- | C. | 溴离子[:$\underset{\stackrel{••}{Br}}{••}$:]- | D. | 钙离子Ca2+ |
分析 A、氯原子的最外层有7个电子;
B、阴离子要表示出最外层电子,且中括号括起来,并标上所带的负电荷;
C、阴离子要表示出最外层电子,且中括号括起来,并标上所带的负电荷;
D、简单阳离子的电子式是其离子符号本身.
解答 解:A、氯原子的最外层有7个电子,故氯原子的电子式为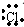 ,故A正确;
,故A正确;
B、阴离子要表示出最外层电子,且中括号括起来,并标上所带的负电荷,故硫离子的电子式为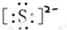 ,故B错误;
,故B错误;
C、阴离子要表示出最外层电子,且中括号括起来,并标上所带的负电荷,故溴离子的电子式为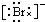 ,故C正确;
,故C正确;
D、简单阳离子的电子式是其离子符号本身,故钙离子的电子式即为Ca2+,故D正确.
故选B.
点评 本题考查了常见化学用语的书写,题目难度中等,明确电子式等概念及书写原则为解答关键,充分考查了学生的灵活应用能力及规范答题能力.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:选择题
| 海水密度(g/mL) | CaSO4 | NaCl | MgCl2 | Mg SO4 | NaBr |
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
| A. | CaSO4 | B. | MgSO4 | C. | NaCl | D. | MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
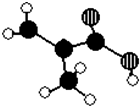 某化工厂生产的某产品A只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).
某化工厂生产的某产品A只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).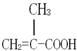 ,用1H核磁共振谱可以证明该化合物的核磁共振氢谱中有3个吸收峰.
,用1H核磁共振谱可以证明该化合物的核磁共振氢谱中有3个吸收峰.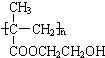 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
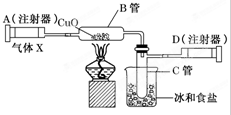 如图所示的实验装置可用来测定含两种元素的气体X的分子式.
如图所示的实验装置可用来测定含两种元素的气体X的分子式.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
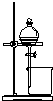 | 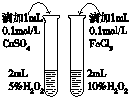 | 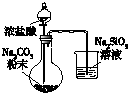 | 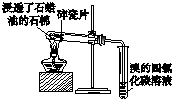 |
| 用于分离苯萃取碘水后的有机层和水层 | 比较不同种催化剂对反应速率的影响 | 验证酸性:H2CO3>H2SiO3 | 证明石蜡油分解生成的气体是乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
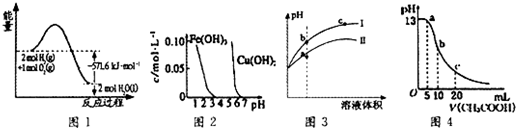
| A. | 图1表示H2与O2发生反应过程中的能量变化,H2的燃烧热为285.8 kJ/mol | |
| B. | 由图2得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入适量CuO,调节溶液的pH至4左右 | |
| C. | 图3表示用水稀释pH相同的盐酸和醋酸时溶液的pH变化曲线,其中Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a | |
| D. | 图4表示常温下向体积为10 mL0.1 mol/LNaOH溶液中逐滴加入0.1 mol/LCH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为18的硫原子:1816S | B. | HClO的结构式为:H-O-Cl | ||
| C. | H2O2的电子式: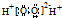 | D. | 聚乙烯的结构简式: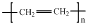 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2既是氧化剂,又是还原剂 | |
| B. | O2是还原产物,Mn2+是氧化产物 | |
| C. | 通常用浓盐酸酸化高锰酸钾溶液 | |
| D. | 标准状况下,产生22.4 L O2时反应转移2 mol e- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com