
【题目】Ⅰ.ClO2气体是一种高效、广谱、安全的杀菌消毒剂,可用NaClO3和草酸(H2C2O4)反应制得。无水草酸100℃可以升华。某学习小组用下图装置模拟工业制取收集ClO2 。

(1)实验时装置A需在60℃~100℃进行的原因是_________,控制所需温度的方法是________。
(2)装置A中反应产物有Na2CO3、ClO2和CO2等,该反应的化学方程式为___________。
(3)在装置C中ClO2和NaOH反应生成等物质的量的两种盐,其中一种盐为NaClO2 ,写出反应的离子方程式_________________。
Ⅱ. 某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡,混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案:
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
浓度(mol/L) | 体积/mL | 浓度(mol/L) | 体积/mL | ||
① | 0.10 | 2.0 | 0.01 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.01 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.01 | 4.0 | 50 |
(1)已知反应后H2C2O4转化为CO2逸出,为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:c(H2C2O4)c(KMnO4) ≥______________。
(2)探究温度对化学反应速率影响的实验编号是_______ (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是________.
(3)实验①测得KMn04溶液的褪色时间为40 s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMn04)=_______mol·L-1·min-1。
【答案】 温度过低,化学反应速率较慢,温度过高草酸升华或分解 水浴加热 2NaClO3+H2C2O4=加热=Na2CO3+2ClO2↑+CO2↑+H2O 2ClO2+2OH-= ClO2-+ ClO3-+H2O 2.5 ②③ ①② 0.01
【解析】Ⅰ.(1)一般来说,升高温度,活化分子的百分数增大,反应速率增大,温度过低,化学反应速率较慢,无水草酸100℃可以升华,温度过高草酸升华或分解,所以实验时装置A需在60℃~100℃进行,反应温度低于水的沸点,用水浴可使反应容器受热均匀,所以反应要用水浴加热;
(2)装置A中反应物为NaClO3、H2C2O4,产物有Na2CO3、ClO2和CO2等,Cl(+5→+4),C(+3→+4),根据得失电子守恒和原子守恒,该反应方程式为:2NaClO3+H2C2O4![]() Na2CO3+CO2↑+2ClO2↑+H2O;
Na2CO3+CO2↑+2ClO2↑+H2O;
(3)NaOH吸收ClO2尾气,生成物质的量之比为1:1的两种阴离子,一种为ClO2-,氧化还原反应规律,另一种离子中Cl元素化合价升高,即为ClO3-,反应的离子方程式为:2ClO2+2OH-=ClO3-+ClO2-+H2O;
Ⅱ.(1)高锰酸钾在酸性环境下能够氧化过氧化氢,生成氧气,高锰酸根离子被还原为二价锰离子,反应中化合价降低的元素是锰元素,从+7价降到+2价,过氧化氢中氧元素化合价从-1价升高到0价,要使得失电子守恒,高锰酸根离子系数为2双氧水系数为5,依据原子个数守恒反应的离子方程式:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O;
(2)探究温度对化学反应速率影响,必须满足除了温度不同,其他条件完全相同,所以满足此条件的实验编号是:②和③;探究反应物浓度对化学反应速率影响,除了浓度不同,其他条件完全相同的实验编号是①和②;
(3)混合后溶液中高锰酸钾的浓度为: ![]() =
=![]() mol/L,40s即
mol/L,40s即![]() min,反应完全时平均反应速率v(KMnO4)=
min,反应完全时平均反应速率v(KMnO4)= ![]() =
=![]() ÷
÷![]() mol/(Lmin)=0.01mol/(Lmin)。
mol/(Lmin)=0.01mol/(Lmin)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列物质分离的方法不正确的是 ( )
A. 用酒精萃取碘水中的碘
B. 用蒸馏的方法将自来水制成蒸馏水
C. 用淘洗的方法从沙里淘金
D. 用过滤的方法除去食盐中的泥沙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将反应Cu(s)+2Ag+(aq)![]() Cu2+(aq)+2Ag(s)设计成如右图所示的原电池,下列叙述正确的是( )
Cu2+(aq)+2Ag(s)设计成如右图所示的原电池,下列叙述正确的是( )

A. KNO3盐桥中的K+移向Cu(NO3)2溶液
B. 该原电池可使用KCl盐桥
C. 工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大
D. 取出盐桥后,电流计的指针依然发生偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)卫星发射时可用肼(N2H4)作燃料,8gN2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出155.5 kJ热量,写出反应的热化学方程式____________________________________。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5 kJ/mol
②NH2CO2NH4(s)= CO(NH2)2(s) +H2O(g) △H=+116.5 kJ/mol
③H2O(l)=H2O(g) △H=+44 kJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式_____________________________。
(3)断裂1 mol化学键所需的能量如表所示:
共价键 | H—N | H—O | N≡N | O==O |
断裂1 mol化学键所需能量/kJ | 393 | 463 | 941 | 496 |
计算1molN2(g)与H2O(g)反应生成NH3(g)和O2(g)的反应热△H = _______________。
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。
I.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请完成以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①在X极附近观察到的现象是_________________;
②电解一段时间后,该反应总离子方程式_______________________________;若用该溶液将阳极产物全部吸收,反应的离子方程式__________________________。
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是____________,电解一段时间后,CuSO4溶液浓度_________(填“增大”、减小”或“不变”)。
(3)若X、Y都是惰性电极,a是溶质为Cu(NO3)2和X(NO3)3,且均为0.1 mol的混合溶液,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是_____。

II.右图为模拟工业离子交换膜法电解饱和食盐水制备烧碱的工作原理。

下列说法正确的是____。
A.从E口逸出的气体是Cl2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH
D.电解一段时间后加适量盐酸可以恢复到电解前的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A. 用于火力发电的煤等化石能源都是不可再生能源
B. 火力发电会产生有害物质,污染环境
C. 火力发电是化学能直接转化为电能的过程
D. 火力发电是化学能间接转化为电能的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A,B,C,D,E,F,G七种元素,试按下述所给的条件推断: ①A,B,C是同一周期的金属元素,已知原子核外有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D,E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的元素.
(1)A的名称是 , B位于周期表中第周期族,C的原子结构示意图是 .
(2)E的单质颜色是 .
(3)A元素与D元素形成化合物的电子式是 .
(4)G的单质与水反应的化学方程式是 .
(5)F的元素符号是 .
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的化学式是 , 酸性最强的化学式是 , 气态氢化物最稳定的化学式是 .
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是有机金属化学中的常用配体,合成F的一种路线如下:

已知:
①A的核磁共振氢谱为三组峰,且峰面积之比为2:1:3; C的核磁共振氢谱为单峰。
②两分子羰基化合物在一定条件下可以发生下列反应:
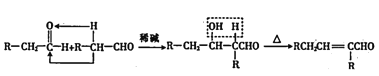
回答下列问题:
(1)A的化学名称是_______。
(2)由A生成B和E生成F的反应类型分别是_____、_______。
(3)B的结构简式为________。
(4)C与D反应生成E的化学方程式为________________。
(5)一定条件下,D与氢气加成后的产物与G互为同系物,且G的分子式为C8H10O。G的同分异构体中,可与FeCl3溶液发生显色反应、核磁共振氢谱为4组峰,且峰面积之比为 6:2:1:1的结构简式为_______、________。
(6)写出以乙醇为原料(其他无机试剂任选)制备化合物CH3CH=CHCHO的合成路线_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com