
| 1 |
| 2 |
| A、①和②产物的阴阳离子个数比不相等 |
| B、①和②生成等物质的量的产物,转移电子数不同 |
| C、25℃、101kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=-317 kJ?mol-1 |
| D、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| 1 |
| 2 |


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
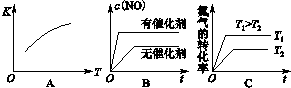
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 结论 |
| A | 在蔗糖中加入几滴水搅拌均匀,再加入浓硫酸,迅速搅拌 | 蔗糖逐渐变黑,体积膨胀,形成疏松多孔的物质 | 体现了浓硫酸的脱水性、氧化性及酸性 |
| B | 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 | 产生红色沉淀 | 淀粉水解可生成葡萄糖 |
| C | 硫酸铵溶液滴入蛋白质溶液中 | 生成白色沉淀 | 蛋白质溶液发生了盐析 |
| D | 苯滴入溴水中并充分振荡,并静置 | 溴水不褪色 | 苯与溴水不发生化学反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蛋白质和糖类都属于天然有机高分子化合物 |
| B、牛奶中蛋白质的含量可通过勾兑三聚氰胺来提高 |
| C、甲醛、酒精或小苏打溶液均能使蛋白质变性 |
| D、可以采用多次盐析或渗析的方法来分离、提纯蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、燃烧反应都是放热反应 |
| B、对于可逆反应:aA(g)+bB(g)?bC(g)+dD(g),如果正反应放热,逆反应一定吸热 |
| C、氢气燃烧生成水是一个放热的化学反应,说明1mol H2的能量高于1mol H2O的能量 |
| D、只有放热的氧化还原反应才可以设计为原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用亚硫酸钠溶液处理纸浆中的残氯:SO32-+2OH-+Cl2═2Cl-+SO42-+H2O |
| B、二氧化硫通入足量的溴水中:SO2+Br2+2H2O═2HBr+2H++SO42- |
| C、硫酸氢铵溶液中滴加少量NaOH溶液:H++NH4++2OH-═NH3?H2O+H2O |
| D、向酸性KMnO4溶液中通入SO2:2MnO4-+5SO2+4OH-═2Mn2++5SO42-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2v(NH3)=v(CO2) |
| B、密闭容器中总压强不变 |
| C、密闭容器中混合气体的平均摩尔质量不变 |
| D、密闭容器中氨气的体积分数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在化学反应中,反应物转化为生成物的同时,必然发生能量的变化 |
| B、氮肥包括铵态氮肥、硝态氮肥和尿素 |
| C、在书写热化学方程式时应标明反应物及生成物的状态,无需标明反应温度和压强 |
| D、医疗上用的石膏绷带是利用熟石膏与水混合成糊状后很快凝固的性质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com