
���� ��1����Ӧ����CԪ�صĻ��ϼ����ߣ�SiԪ�صĻ��ϼ۽��ͣ�
��2����Ӧ����ClԪ�صĻ��ϼ۽��ͣ��÷�Ӧ���ᴿSi��
��3���ɷ�Ӧ�٢ڢۿ�֪��2C��2Cl2��Si���Դ˼��㣮
��� �⣺��1����Ӧ����CԪ�صĻ��ϼ����ߣ�SiԪ�صĻ��ϼ۽��ͣ���CΪ��ԭ����SiO2Ϊ���������ʴ�Ϊ��SiO2��C��
��2����Ӧ����ClԪ�صĻ��ϼ۽��ͣ�Cl2������������������Si��Ҫ�ٴ����ɻ���̬���ԭ�����ᴿSi���ʴ�Ϊ�������������ᴿSi��
��3���ɷ�Ӧ�٢ڢۿ�֪��2C��2Cl2��Si��ÿ����14kg�ߴ��裬���������Ľ�̿����Ϊ14kg��$\frac{12��2}{28}$=12kg��Cl2������Ϊ14kg��$\frac{2��71}{28}$=71kg���ʴ�Ϊ��12��71��
���� ���⿼��������ԭ��Ӧ��Ϊ�߿��������ͺ�Ƶ���㣬���շ�Ӧ��Ԫ�صĻ��ϼ۱仯�����ʵ�����ϵΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
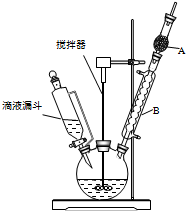 �����״���C6H5��3C-OH��һ����Ҫ�Ļ���ԭ�Ϻ�ҽҩ�м��壮ʵ���Һϳ������״���ʵ��װ����ͼ��ʾ��
�����״���C6H5��3C-OH��һ����Ҫ�Ļ���ԭ�Ϻ�ҽҩ�м��壮ʵ���Һϳ������״���ʵ��װ����ͼ��ʾ��| ���� | �е�/�� |
| �����״�[ | 380 |
| ���� | 34.6 |
| �屽 | 156.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��

| A�� | ͼ���ĵ�Kw��Ĺ�ϵ��A=D��C��B | |
| B�� | ����A�㵽D�㣬�ɲ��ã��¶Ȳ�����ˮ�м������� | |
| C�� | ����A�㵽C�㣬�ɲ��ã��¶Ȳ�����ˮ�м�����NaAc���� | |
| D�� | ����A�㵽D���ɲ��ã��¶Ȳ�����ˮ�м�����NaAc���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4NA | B�� | 3NA | C�� | 2NA | D�� | NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H+��Ba2+��Cl-��NO3- | B�� | K+��AlO2-��Cl-��SO42- | ||
| C�� | Ca2+��Mg2+��NO3-��HCO3- | D�� | Fe3+��NH4+��SCN-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������� | |
| B�� | H2O2�ֽⲻ��ȫ | |
| C�� | Na2O2ת��ΪNa0H��H2O2�ķ�Ӧ����ȫ | |
| D�� | װ��©�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com