
��֪һ�������¶��ѻ��γ�ijЩ��ѧ����������ϵ���±���
| ���ѻ��γɵĻ�ѧ�� | �������� |
| ����1 mol H2�����еĻ�ѧ�� | ��������436 kJ |
| ����1 mol Cl2�����еĻ�ѧ�� | ��������243 kJ |
| �γ�1 mol HCl�����еĻ�ѧ�� | �ͷ�����431 kJ |
���ڷ�Ӧ��H2(g)��Cl2(g)===2HCl(g)������˵����ȷ����(����)
A���÷�Ӧ�ķ�Ӧ�Ȧ�H>0
B������1 mol HClʱ��Ӧ����431 kJ
C�����������еĻ�ѧ�������������еĻ�ѧ�����ι�
D����ͬ�����£��������Ӿ��е����������������Ӿ��е�����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʽΪC7H16�������У�����3������ͬ���칹����Ŀ�� ( )
A��2�� B��3�� C��4�� D��5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ʵ�����A��B�����2 L���ܱ������У��������·�Ӧ��
3A(g)��B(g) xC(g)��2D(g)����5 min���D��Ũ��Ϊ0.5 mol/L��c(A)��c(B)��3��5��
xC(g)��2D(g)����5 min���D��Ũ��Ϊ0.5 mol/L��c(A)��c(B)��3��5��
C��ƽ����Ӧ����Ϊ0.1 mol/(L��min)��ͨ��������
��1����Ӧ��ʼǰ�����е�A��B�����ʵ�����
��2��B��ƽ����Ӧ���ʣ�
��3��x��ֵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ClCH2COONa�Ǻϳ�һ�ֳ��ݼ�����Ҫԭ�ϣ����Ʊ��������£�
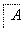
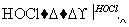

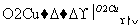
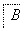
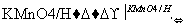
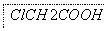
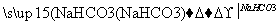
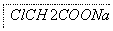
��ش��������⣺
(1)��֪��A����Է�������Ϊ28���������ʽΪ__________����Ӧ�ٵ��л���Ӧ����Ϊ________________��
(2)��A��һ�������·����ۺϷ�Ӧ�����ɸ߷��ӻ������Ӧ�Ļ�ѧ����ʽΪ________________��
(3)��Ӧ���������Ҵ��Ĵ���������Ӧ�Ļ�ѧ����ʽΪ______��
(4)��Ũ����������£�ClCH2CH2OH��ClCH2COOH�ɷ�����Ӧ���÷�Ӧ�������Ҵ��������������Ӧ����Ӧ�Ļ�ѧ����ʽΪ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Cu2O��һ�ְ뵼����ϣ�������ɫ��ѧ������Ƶ���ȡCu2O�ĵ���ʾ��ͼ��ͼ��ʾ������ܷ�ӦΪ2Cu��H2O===Cu2O��H2��������˵����ȷ����(����)
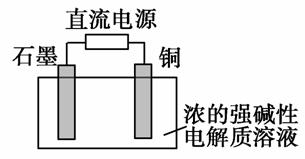
A��ʯī�缫�ϲ�������
B��ͭ�缫������ԭ��Ӧ
C��ͭ�缫��ֱ����Դ�ĸ���
D������0.1 mol����ת��ʱ����0.1 mol Cu2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��H2(g)��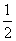 O2(g)===H2O(g)����H1����241.8 kJ��mol��1��C(s)��
O2(g)===H2O(g)����H1����241.8 kJ��mol��1��C(s)��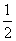 O2(g)===CO(g)����H2����110.5 kJ��mol��1���ɴ˿�֪��̿��ˮ������Ӧ���Ȼ�ѧ����ʽΪ��C(s)��H2O(g)===CO(g)��H2(g)����H3����H3Ϊ(����)
O2(g)===CO(g)����H2����110.5 kJ��mol��1���ɴ˿�֪��̿��ˮ������Ӧ���Ȼ�ѧ����ʽΪ��C(s)��H2O(g)===CO(g)��H2(g)����H3����H3Ϊ(����)
A����131.3 kJ��mol��1���������� B����131.3 kJ��mol��1
C����352.3 kJ��mol��1 D����352.3 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��ȤС����������ʵ�飺ȡ��֧�Թܣ��Թ�A�м���Լ1 g Na2CO3�����ĩ���Թ�B�м���Լ1 g NaHCO3�����ĩ�������Թ���ͬʱ����Լ2 mL 3 mol/L������۲�������Ӧֹͣ�����ִ������Թ���ڡ�
ʵ�������¼���£�
�����Թ��еķ�Ӧ���Ͽ죬������ɫ��ζ�����壬���Թ�B��Ӧ�����ң�
�ڷ�Ӧֹͣ�����ִ����Թ���ڣ������Թ�A���ȣ��Թ�B��ñ�����
��С��ͬѧ�������ϣ��õ���Na2CO3(aq)�����ᷴӦ�����е������仯ʾ��ͼ���¡�
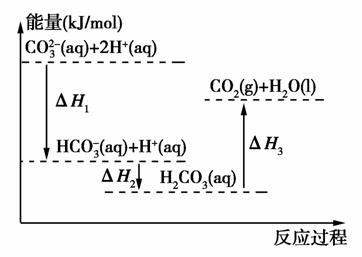
(ע��̼������̼�����Ƶ��ܽ���̵���ЧӦ���Բ���)
��ش��������⣺
(1)Ϊʲô�Թ�B�в������ݵ����ʸ��죿__________________��
(2)��д��CO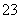 ��H����Ӧ����CO2��H2O���Ȼ�ѧ����ʽ��________________��
��H����Ӧ����CO2��H2O���Ȼ�ѧ����ʽ��________________��
(3)��ͬ�����£����H����������CO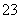 ________HCO
________HCO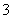 (�>������������<��)��
(�>������������<��)��
(4)HCO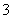 ��H��===CO2����H2O��һ��________(������š�)�ȷ�Ӧ���÷�Ӧ�ڳ��³�ѹ�����Է����е�ԭ����________��
��H��===CO2����H2O��һ��________(������š�)�ȷ�Ӧ���÷�Ӧ�ڳ��³�ѹ�����Է����е�ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2 mol A��1 mol B����V�����ܱ������У���һ�������·�����Ӧ��2A(g)��B(g)2C(g)��ƽ��ʱC���������(%)���¶Ⱥ�ѹǿ�ı仯���±���ʾ��
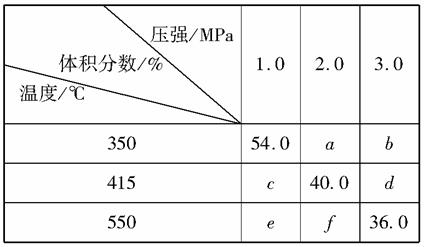
�����ж���ȷ����(����)
A��b>e
B��415 �桢2.0MPaʱB��ת����Ϊ60%
C���÷�Ӧ�Ħ�H>0
D��ƽ�ⳣ��K(550 ��)>K(350 ��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ũ�Ȼ����Һ����������̨Ļ�������Ż���ԭ���� (����)
��Ļ�����Ż�����ߡ���Ļ�����������ӡ����Ȼ�立ֽ������������������¶ȡ����Ȼ�立ֽ��������������˿���
A���٢� B���ۢ� C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com