

���� ��ʵ��ԭ���ǣ����ݻ�ͭ�����ȷֽ�����Ķ�����������IJⶨ��������������õ�ˮ���궨�������Ԫ���غ����ȷ����ͭ����������������䴿�ȣ�
��1���������ı�������Լӿ컯ѧ��Ӧ���ʣ�
��2��Ũ������Խ�ˮ��ȥ�������Ը���ð�����ݵ����������ڿ������٣����ȵ�ͭ�����Գ�ȥ�����������
��3����������ȫ����������ʵ��ɰܵĹؼ���
��4����֪�����ķ�Ӧ��8CuFeS2+21O2$\frac{\underline{\;����\;}}{\;}$8Cu+4FeO+2Fe2O3+16SO2��I2+SO2+2H2O�TH2SO4+2HI���������ĵĵⵥ�ʵ����ʵ������CuFeS2�����ʵ������������ٸ�����Ʒ�������������������
��5����������͵��ʵ�֮�䷢��������ԭ��Ӧ���������ĵⵥ�ʵ�������ȷ�������������������ȷ����ͭ��Ĵ��ȣ�
��6��������̼�Ͷ�����������Ժ�����������Ӧ���ɰ�ɫ�����������ᱵ�ױ�����Ϊ���ᱵ��
��� �⣺��ʵ��ԭ���ǣ����ݻ�ͭ�����ȷֽ�����Ķ�����������IJⶨ��������������õ�ˮ���궨�������Ԫ���غ����ȷ����ͭ����������������䴿�ȣ�
��1������Ʒ��ϸ���ٷ�Ӧ�����������ı������Ŀ����ʹԭ�ϳ�ַ�Ӧ���ӿ췴Ӧ���ʣ�
�ʴ�Ϊ������Ӵ������ʹԭ�ϳ�ַ�Ӧ���ӿ췴Ӧ���ʣ�
��2��װ��a�е�Ũ����������տ����е�ˮ������ͬʱ����ð�������ݵ����������������ͨ���������ȵ�ͭ�����Գ�ȥ������������ʴ�Ϊ��bd��e��
��3����ͭ�����ȷֽ����ɶ��������һϵ�в���ֽ���Ϻ���Ȼͨ����������Խ������Ķ�������ȫ���ų�ȥ��ʹ�����ȷ��
�ʴ�Ϊ��ʹ��Ӧ���ɵ�SO2ȫ������dװ���У�ʹ�����ȷ��
��4����֪�����ķ�Ӧ��8CuFeS2+21O2$\frac{\underline{\;����\;}}{\;}$8Cu+4FeO+2Fe2O3+16SO2��I2+SO2+2H2O�TH2SO4+2HI��
��0.05mol/L������Һ���еζ������ı���Һ20mL�������ĵĵⵥ�ʵ���Ϊ��0.05mol/L��0.02L=0.0010mol��
���ݷ�Ӧ����ʽ�õ���2I2��2SO2��CuFeS2�����Ի�ͭ��������ǣ�0.0010mol��$\frac{1}{2}$��184g/mol��10=0.92g��
�����䴿���ǣ�$\frac{0.92g}{1.84g}$��100%=50%��
�ʴ�Ϊ��50%��
��5������ͼ2װ���������ʵ��װ��d�������âۣ�ԭ����ǰ��ͨ��Ŀ�����Ҳ��ռ��һ��������������������ᱵ�ܹ����ն�����������Һ�������仯������������������
�ʴ�Ϊ���ڣ�
��6�������е�CO2��Ba��OH��2��Ӧ��������BaCO3����������BaSO3��������BaSO4�����Ե������Եij��������ȶ������������������Ӧ���ɵİ�ɫ���������࣬
�ʴ�Ϊ�������е�CO2��Ba��OH��2��Ӧ����BaCO3������BaSO3��������BaSO4��
���� ���⿼����̽����ͭ��Ĵ��ȣ��漰��ʵ��ԭ���ķ���Ӧ�á����ȼ��㡢ʵ�鷽�������۵�֪ʶ����Ŀ�Ѷ��еȣ�������ؿ���ѧ���ķ������������������Ӧ�û���֪ʶ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18O2��16O2�����ֲ�ͬ��ԭ�� | B�� | �״���CH3OH���������ӻ����� | ||
| C�� | N5��N2�ǵ�Ԫ�ص�����ͬλ�� | D�� | ��N5���N2�ǻ�ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

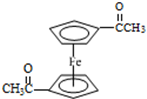 ��������ʹ�õ���������������������˴Ź������ף�
��������ʹ�õ���������������������˴Ź������ף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ����������������ͨ�뵽Ư����Һ�У�Ca2++2ClO-+SO2+H2O=CaSO3��+2HClO | |
| B�� | ��Fe��OH��3�������Fe��OH��3+3H+=Fe3++3H2O | |
| C�� | ��������Ͷ��������ˮ�У�2Na+2H2O=2Na++2OH-+H2�� | |
| D�� | ������������Һ�е�������������Һ��pH=7 Ba2++2OH-+2H++SO42-=BaSO4��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ��� | A | B | C | D |
| ʵ�� ���� | 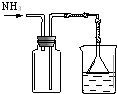 |  | 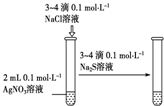 |  ���ڹ����� |
| ʵ�� Ŀ�� | �ռ������������� β������ | ��ȡ��Ȳ����֤Ȳ�� ������ | ��֤AgCl������ת��Ϊ �ܽ�ȸ�С��Ag2S���� | ��֤����������������ѧ��Ӧ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ζ�ǰ������ʹ�����Һ�У�c��Cl?����c��CH3COO-�� | |
| B�� | �ֱ����10.00 mL NaOH��Һʱ����ô��ᷴӦ��������ҺpH=6������Һ��$\frac{c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$��1 | |
| C�� | ��������Һ��pH������7ʱ��������������NaOH��Һ�������ȣ��������ĵ�NaOH��Һ����� | |
| D�� | ����20.00 mL NaOH��Һʱ������������Һ�У�c��Cl?����c��CH3COO-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
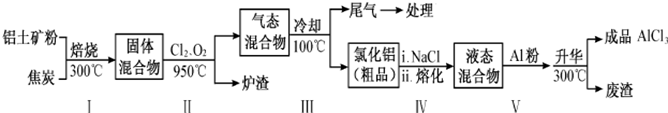
| ���� | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
| �е�/�� | 57.6 | 180�������� | 300�������� | 1023 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com