
【题目】10mLNO、CO2 的混合气体通过足量的Na2O2后,气体的体积变为6 mL (相同状况),则NO和CO2的体积比为( )
A.1:1B.2:1C.3:2D.1:2
【答案】D
【解析】
发生反应有:①2Na2O2+CO2==Na2CO3 + O2 ,② 2NO+ O2==2NO2,问题的关键在于NO与氧气反应存在着三种可能性,一种情况是恰好反应,一种情况是NO过量,另一O2种情况可能是过量,据此讨论计算。
发生反应有:①2Na2O2+2CO2═2Na2CO3+O2,②2NO+O2═2NO2,
假设参加反应的CO2为x mL,NO为y mL,则x+y=10,
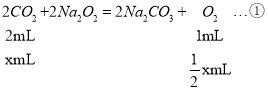
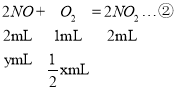
(1)当反应②恰好反应时,即当y=x时(此时x、y都等于5),生成的NO2的体积为5mL,不符合题意,所以选项A错误;
(2)当y>x时,NO有过量,O2反应完,此时反应掉的NO为xmL,则剩余的NO为(ymL-xmL),生成的NO2气体为xmL,因此,反应最后得到的混合气体为NO和NO2,其体积和为:(ymL-xmL)+xmL=ymL,故y=6ml,即NO体积6ml,结合x+y=10,x=4ml,则CO2为4 mL,故NO和CO2的体积比为6ml:4ml=3:2,故B错误,C正确;
(3)当y<x时,NO不足,O2过量,此时反应掉的O2为![]() mL,剩余的O2为(
mL,剩余的O2为(![]() mL-
mL-![]() mL),生成的NO2气体为ymL.因此,反应最后得到的混合气体为O2和NO2,其体积和为:(
mL),生成的NO2气体为ymL.因此,反应最后得到的混合气体为O2和NO2,其体积和为:(![]() mL-
mL-![]() mL)+ymL=
mL)+ymL=![]() mL+
mL+![]() mL=5mL,这与题意“气体体积缩小为6mL”不符合,这表明如果y<x,这种情况不符合题意,所以选项D错误;
mL=5mL,这与题意“气体体积缩小为6mL”不符合,这表明如果y<x,这种情况不符合题意,所以选项D错误;
故答案为C。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大。在如图所示的物质转化关系中,p、q、m、n分别是元素W、X、Y、Z的气体单质,p和s均为有色气体,v的水溶液呈碱性。常温,0.1mol/Lt溶液与0.1mol/L u溶液的pH均为1,下列说法正确的是( )
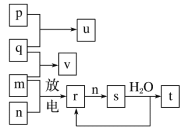
A. 元素的非金属性:Z>Y>X,原子半径:X<Z<Y
B. Y、W的氧化物对应的水化物均为强酸
C. s溶于水的反应中,氧化剂与还原剂的物质的量之比为2∶1
D. v的电子式可表示为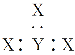
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表代表周期表中的几种短周期元素,下列说法中错误的是

A. A、B、C第一电离能的大小顺序为C>B>A
B. C、D气态氢化物稳定性强弱和沸点高低均为C>D
C. AD3和ED4两分子的中心原子均为sp3杂化
D. ED4分子中各原子均达8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号 | I | II | III |
实验步骤 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
下列说法不正确的是
A. 实验I、II、III中均涉及Fe3+被还原
B. 对比实验I、II说明白色沉淀的产生与铜粉的量有关
C. 实验II、III中加入蒸馏水后c(Cu2+)相同
D. 向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某火电厂收捕到的粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等。研究小组对其进行综合处理的流程如下:
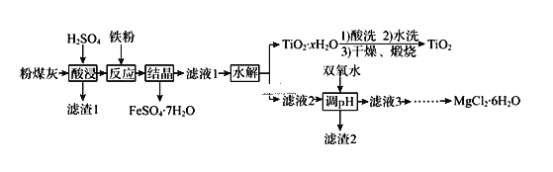
已知:①常温下,Ksp[Al(OH)3] ≈ 8.0×10-35;②滤液1中仍有Fe2+剩余③Fe3+完全沉淀时pH为3.7;Al3+完全沉淀时pH为5.0;Fe2+完全沉淀时pH为9.7;
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有_________(任写两种)。
(2)怎样判断TiO2xH2O沉淀已经洗涤干净________________________________。
(3)加入双氧水的目的是_____________________________________。滤渣2中的成分分别为Al(OH)3和_______________,Al(OH)3沉淀完全时(溶液中离子浓度小于10-5mol/L),溶液中的c(OH-)为________。
(4)将MgCl26H2O制成无水MgCl2时应注意__________________________________。
(5)某同学以石墨为两个电极,电解MgCl2溶液以制取金属镁。你认为他能否获得成功?_______。用化学方程式解释原因___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(FeSO4·7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:
![]()
已知:FeS2和铁黄均难溶于水。下列说法错误的是( )
A.步骤①后可依次用KSCN溶液和酸性KMnO4溶液来检测溶液中铁元素的价态
B.步骤②发生后,溶液的酸性增强
C.步骤③,将溶液蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥可得到绿矾
D.为确保铁黄的产率,尽可能将步骤④中的pH值调大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图每一方格表示有关的一种反应物或生成物,其中A、C为无色气体,D气体能使带火星的木条复燃,X是一种常见的酸式盐。
试填写下列空白:
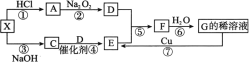
(1) 物质X的名称是___________;检验C气体的方法是___________。
(2) 反应④的化学方程式为___________。
(3) 反应⑥中氧化剂与还原剂的质量之比为___________;反应⑦中氧化剂与还原剂的物质的量之比为___________。
(4) 写出X与足量NaOH溶液反应的离子方程式:____________。
(5) 在标准状况下,在一个干燥的烧瓶内F和D的混合气体[V(F)∶V(D)=4∶1]。然后做喷泉实验,则烧瓶中所得溶液中溶质的物质的量浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置中,A是用二氧化锰制取氯气发生装置,C、D为气体净化装置(C中装有饱和食盐水,D中装有浓硫酸),E是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G中装有氢氧化钠溶液。
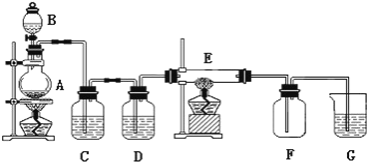
请回答下列问题:
(1)仪器B的名称是________________;
(2)实验室制氯气的化学方程式:________________;
(3)C装置的作用是________________;D装置的作用是________________;
(4)E中发生化学反应的方程式为:________________;
(5)烧杯G中发生反应的化学方程式为:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式如下图所示,下列说法正确的是
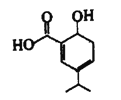
A. 分子式为C10H12O3 B. 能使酸性KMnO4溶液或溴水褪色
C. lmol该有机物可中和2molNaOH D. 1mol该有机物最多可与3molH2发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com