
【题目】常温下将NaOH溶液滴加到H2X溶液中,混合溶液的pH与![]() 、
、![]() 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是

A. H2X为二元强酸
B. 当![]() =1时,溶液中c(HXˉ)=c(H2X)
=1时,溶液中c(HXˉ)=c(H2X)
C. NaHX溶液中c(H+)<c(OHˉ)
D. 当溶液pH=4.6时c(HXˉ)>c (X2-)
【答案】D
【解析】当![]() =0时,c(HX-)/c(H2X)=1,此时pH≈4.4,Ka1(H2X)≈10﹣4.4;当lg
=0时,c(HX-)/c(H2X)=1,此时pH≈4.4,Ka1(H2X)≈10﹣4.4;当lg![]() =0时,
=0时,![]() =1,此时pH≈5.4,Ka2(H2X)≈10﹣5.4;所以H2X为二元弱酸;A错误;当
=1,此时pH≈5.4,Ka2(H2X)≈10﹣5.4;所以H2X为二元弱酸;A错误;当![]() =1时,c(HX-)/c(H2X)=10,c(HX-)=10 c(H2X),B错误;NaHX属于强碱弱酸盐,水解平衡常数为Kh=KW/ Ka1(H2X)=10-14/10﹣4.4=10-9.6;而HX-的电离平衡常数为Ka2(H2X)≈10﹣5.4,Kh< Ka2(H2X),所以电离过程大于水解过程,NaHX显酸性,c(H+)>c(OHˉ),C错误;当溶液pH=4.6时,lg
=1时,c(HX-)/c(H2X)=10,c(HX-)=10 c(H2X),B错误;NaHX属于强碱弱酸盐,水解平衡常数为Kh=KW/ Ka1(H2X)=10-14/10﹣4.4=10-9.6;而HX-的电离平衡常数为Ka2(H2X)≈10﹣5.4,Kh< Ka2(H2X),所以电离过程大于水解过程,NaHX显酸性,c(H+)>c(OHˉ),C错误;当溶液pH=4.6时,lg![]() =-0.8,c(X2-)/c(HX-)=10-0.8,所以c(HXˉ)>c (X2-),D正确;正确选项D。
=-0.8,c(X2-)/c(HX-)=10-0.8,所以c(HXˉ)>c (X2-),D正确;正确选项D。


科目:高中化学 来源: 题型:
【题目】现有如下两个反应:(A)NaOH+HCl===NaCl+H2O (B)2FeCl3+Cu===2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)(A)______,(B)________;
(2)如果(A或B)不能,说明其原因_________________________________________;
(3)如果(A或B)可以,则在下面方框中画出装置图并写出正、负极材料及电极反应式
________
负极:________、_______________________________________;
正极:________、________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图。下列对该实验的描述错误的是

A. 不能用水浴加热
B. 长玻璃管起冷凝回流作用
C. 为提纯乙酸丁酯,可用水和碳酸钠溶液洗涤
D. 通常加入过量1-丁醇以提高乙酸的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料,可制作燃料电池. 
(1)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=﹣1275.6kJmol﹣1②2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJmol﹣1
③H2O(g)=H2O(l)△H3=﹣44.0kJmol﹣1写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)CO(g)+3H2(g) ①一定条件下CH4的平衡转化率与温度、压强的关系如图a.则,P1P2;A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为 . (填“<”、“>”“=”)
②100℃时,将1mol CH4和2mol H2O通入容积为1L 的反应室,反应达平衡的标志是: .
A.容器内气体密度恒定
B.单位时间内消耗0.1mol CH4同时生成0.3mol H2
C.容器的压强恒定
D.3v正(CH4)=v逆(H2)
③如果达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K=
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为 . 用该原电池做电源,常温下,用惰性电极电解200mL饱和食盐水(足量),消耗标准状况下的CO 224mL,则溶液的pH= (不考虑溶液体积的变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]﹣ , 铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法. 【方法一】还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.具体流程如下:![]()
有关离子完全沉淀的pH如下表:
有关离子 | Fe2+ | Fe3+ | Cr3+ |
完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(1)写出Cr2O72﹣与FeSO4溶液在酸性条件下反应的离子方程式 .
(2)还原+6价铬还可选用以下的试剂(填序号).
A.明矾
B.铁屑
C.生石灰
D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4 , 再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.则在操作②中可用于调节溶液pH的试剂为:(填序号); A.Na2O2 B.Ba(OH)2 C.Ca(OH)2
此时调节溶液的pH范围在(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
(4)【方法二】电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去. 写出阴极的电极反应式 .
(5)电解法中加入氯化钠的作用是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,请回答有关问题:
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1) 表中化学性质最不活泼的元素,其原子结构示意图为________________。
(2) 表中能形成两性氢氧化物的元素是________(填元素名称),写出该元素的单质与⑨最高价氧化物的水化物反应的离方程式____________________________________。
(3) ①、④、⑤、⑥、⑦、⑨六种元素的最高价氧化物的水化物中,按碱性减弱酸性增强的顺序排列为_____________________________________________(用化学式表示)。
(4) ③元素与⑩元素两者核电荷数之差是_____________________________。
(5) 请写出②的氢化物发生催化氧化的化学方程式_______________________________。
(6) 请写出⑤元素的最高价氧化物与⑥元素的最高价氧化物的水化物反应的离子方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)A和B反应生成C,假定反应刚开始只有A、B,它们的起始浓度均为1mol/L。反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L。则在这2 min内反应的平均速率VA =_______ mol/(L· min),VB =________ mol/(L· min),该反应2 min内A、B、C三种物质的化学反应速率之比为:________________________。
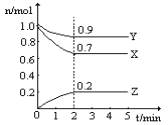
(2)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如上图所示。根据图中数据,试填写下列空白:
①该反应的化学方程式为__________________________________________________;
②从开始至2min,Z的平均反应速率为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为2×(﹣57.3)kJ/mol
B.CO(g)的燃烧热是283.0 kJ/mol,则表示CO燃烧热的热化学方程式为CO(g)+ ![]() O2(g)═CO2 (g);△H=﹣283.0kJ/mol
O2(g)═CO2 (g);△H=﹣283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol硫燃烧生成气态三氧化硫所放出的热量是硫磺的燃烧热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com