
| A. | H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | 将稀硝酸滴加到氯化银固体上:AgCl+H+═Ag++HCl | |
| C. | 澄清的石灰水与稀盐酸反应:H++OH-═H2O | |
| D. | 大理石溶于醋酸的反应:CaCO3+2H+═Ca2++CO2↑+H2O |
分析 A.不符合离子的配比;
B.不发生反应;
C.反应生成氯化钙和水;
D.醋酸在离子反应中保留化学式.
解答 解:A.H2SO4与Ba(OH)2溶液反应的离子反应为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故A错误;
B.将稀硝酸滴加到氯化银固体上,不反应,故B错误;
C.澄清的石灰水与稀盐酸反应的离子反应为H++OH-═H2O,故C正确;
D.大理石溶于醋酸的反应的离子反应为CaCO3+2CH3COOH═2CH3COO-+Ca2++CO2↑+H2O,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质及电荷守恒,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. |  分馏装置 | B. | 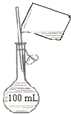 配制150 mL 0.10 mol•L-1盐酸 | ||
| C. |  烧瓶内溶液变蓝色 | D. |  出现砖红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K1=K2 | B. | K1=$\frac{1}{{K}_{2}}$ | C. | K1=(K2)2 | D. | K1=($\frac{1}{{K}_{2}}$)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(s) | 0 | 10 | 20 | 25 | 30 |
| 条件A[n(NO2)](mol) | 0.20 | 0.14 | 0.13 | 0.13 | 0.13 |
| 条件B[n(NO2)](mol) | 0.20 | 0.10 | 0.10 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在空气中,金属银的表面生成一层黑色物质 | |
| B. | 镀银的铁制品,镀层部分受损后,露出的铁表面易被腐蚀 | |
| C. | 埋在潮湿疏松土壤里的铁管比埋在干燥致密不透气的土壤里的铁管更易被腐蚀 | |
| D. | 为保护海轮的船壳,常在船壳上镶入锌块 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ③④⑤ | C. | ①③⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
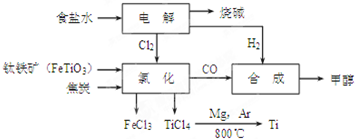
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com