
| A. | 向稀HNO3中滴加Na2SO3溶液:2H++SO32-═SO2↑+H2O | |
| B. | 向Al2(SO4)3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| C. | 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O | |
| D. | 向0.1mol/LpH=1的KHA溶液中加入KOH溶液:H++OH-═H2O |
分析 A.不符合反应客观事实,二者发生氧化还原反应;
B.氢氧化钠过量,二者反应生成偏铝酸钠和水;
C.草酸为弱酸应保留化学式;
D.二者反应生成K2A和水.
解答 解:A.向稀HNO3中滴加Na2SO3溶液:2H++2NO3-+3SO32-═3SO42-+H2O+2NO↑,故A错误;
B.向Al2(SO4)3溶液中加入过量的NaOH溶液,离子方程式:Al3++4OH-=AlO2-+2H2O,故B错误;
C.用高锰酸钾标准溶液滴定草酸,离子方程式:2MnO4-+6H++5H2C2O4═2Mn2++10CO2↑+8H2O,故C错误;
D.向0.1mol/LpH=1的KHA溶液中加入KOH溶液,离子方程式:H++OH-═H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意化学式拆分、注意反应必须遵循客观事实,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 室温下,NaR溶液的pH大于7 | |
| B. | 25℃时,0.01mol/L的HR溶液pH=2.8 | |
| C. | 加热NaR溶液时,溶液的pH变小 | |
| D. | HR溶液加入少量NaR固体,溶解后溶液的pH变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
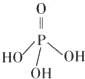 磷元素的单质及其化合物在生产和生活中有着广泛的应用.
磷元素的单质及其化合物在生产和生活中有着广泛的应用.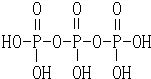 .
.| 电离常数(25℃) |
| HF:Ki=3.6×10 -4 |
| H3PO4:Ki1=7.5×10 -3, Ki2=6.2×10 -8,Ki3=2.2×10 -13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 研究人员研制出一种可在一分钟内完成充放电的超长性能铝离子电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,其放电工作原理如图所示.下列说法正确的是( )
研究人员研制出一种可在一分钟内完成充放电的超长性能铝离子电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,其放电工作原理如图所示.下列说法正确的是( )| A. | 放电时,电子由石墨(Cn)电极经用电器流向铝电极 | |
| B. | 放电时,有机阳离子向铝电极方向移动 | |
| C. | 充电时,铝电极上发生氧化反应 | |
| D. | 放电时,负极的电极反应为:Al-3e-+7AlCl4-═4Al2Cl7- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
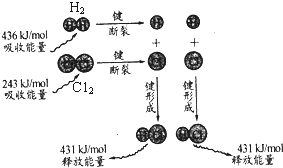
| A. | 2 mol 气态氢原子的能量低于1 mol 氢气 | |
| B. | 氢气分子中的化学键比氯气分子中的化学键更稳定 | |
| C. | 氢气与氯气反应的热化学方程式为H2(g)+C12(g)→2HCl(g)+183 kJ | |
| D. | 该反应在光照和点燃条件下的反应热效应是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
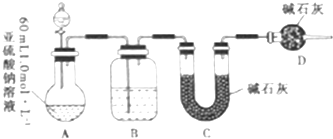
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br2+2NaI=2NaBr+I2 | |
| B. | 2P+8H2O+5Br2=2H3PO4+10HBr↑ | |
| C. | 3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑ | |
| D. | SO2+2H2O+Br2=H2SO4+2HBr |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com