
| A. | 非金属元素之间只能形成共价化合物 | |
| B. | 第IA族元素的金属性一定比IIA族元素的金属性强 | |
| C. | 短周期中,同周期元素的离子半径从左到右逐渐减小 | |
| D. | 非金属元素的气态氢化物还原性越强,对应元素的最高价含氧酸酸性越弱 |
分析 A.非金属元素可形成离子化合物;
B.同周期第IA族元素的金属性一定比IIA族元素的金属性强;
C.同周期阴离子的半径大于阳离子的半径;
D.非金属性越强,对应氢化物越稳定、氢化物的还原性越弱,对应最高价含氧酸酸性越强.
解答 解:A.非金属元素可形成离子化合物,如铵盐为离子化合物,故A错误;
B.同周期第IA族元素的金属性一定比IIA族元素的金属性强,不同周期时金属性无此规律,如金属性Ca>Na,故B错误;
C.同周期阴离子的半径大于阳离子的半径,如第三周期中阴离子半径大于阳离子半径,且铝离子半径最小,故C错误;
D.非金属性越强,对应氢化物越稳定、氢化物的还原性越弱,对应最高价含氧酸酸性越强,则非金属元素的气态氢化物还原性越强,对应元素的最高价含氧酸酸性越弱,如还原性H2S>HCl,酸性为硫酸<高氯酸,故D正确;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的性质、元素周期律、化学键为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 理论解释 | 结论 |
| A | H-N的键能大于H-P | 沸点:NH3>PH3 |
| B | 离子半径:Mg2+<Ba2+ | 热分解温度:碳酸镁髙于碳酸钡 |
| C | 离子半径:Na+<Cs+ | 配位数(C.N.):NaCl<CsCl |
| D | 晶格能:FeS2>ZnS | 岩浆中的硫化物矿物析出顺序ZnS先于FeS2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol Al3+含有的核外电子数为3NA | |
| B. | 将5.85 g NaCl溶于100g水中,所得NaCl溶液的浓度为1.00mol•L-1 | |
| C. | 1 mol Cl2与足量的铁反应,转移的电子数为2NA | |
| D. | 常温下,pH=1的硫酸溶液中含有的H+数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
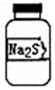 实验室现有一瓶标签右半部分已被腐蚀的固体M,剩余部分只看到“Na2S”字样(如图所示).已知固体M只可能是Na2SO3、Na2SiO3、Na2SO4中的一种.若取少量固体M配成稀溶液进行下列有关实验,其中说法正确的是( )
实验室现有一瓶标签右半部分已被腐蚀的固体M,剩余部分只看到“Na2S”字样(如图所示).已知固体M只可能是Na2SO3、Na2SiO3、Na2SO4中的一种.若取少量固体M配成稀溶液进行下列有关实验,其中说法正确的是( )| A. | 往溶液中通入二氧化碳,若有白色沉淀,则固体M为Na2SiO3 | |
| B. | 往溶液中加入稀盐酸酸化的BaCl2,若有白色沉淀,则固体M为Na2SO4 | |
| C. | 用pH试纸检验,若pH=7,则固体M不一定是Na2SO4 | |
| D. | 只用盐酸一种试剂不能确定该固体M的具体成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充电时,反应每生成1mol H+时电子转移的物质的量为1mol | |
| B. | 放电过程中,正极附近溶液的酸性减弱 | |
| C. | 放电时,正极反应为VO2++2H++e-═VO2++H2O | |
| D. | 充电时,阴极附近溶液由紫色逐渐变为绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 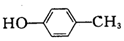 对甲苯酚 属于芳香化合物 对甲苯酚 属于芳香化合物 | B. | 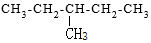 3-甲基戊烷 属于烷烃 3-甲基戊烷 属于烷烃 | ||
| C. | 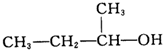 2-甲基-1-丙醇-元醇 2-甲基-1-丙醇-元醇 | D. | 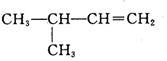 3-甲基-1-丁烯 属于脂肪烃 3-甲基-1-丁烯 属于脂肪烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
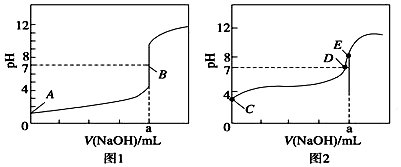
| A. | 根据图1和图2判断,滴定HBr溶液的曲线是图1 | |
| B. | a=20.00 mL | |
| C. | c(Na+)=c(CH3COO-)的点是B点 | |
| D. | E点对应溶液中离子浓度由大到小的顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2$\stackrel{HCI(ap)}{→}$SiCl4$→_{高温}^{H_{2}}$Si | |
| B. | FeS2$→_{煅烧}^{O_{2}}$SO2$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCI(ap)}{→}$NH4Cl(aq) | |
| D. | Al2O3$\stackrel{HCI(ap)}{→}$AlCl3(aq) $\stackrel{电解}{→}$ Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Al3+、Cl-、OH- (5:1:4:4) | B. | NH4+、Ba2+、OH-、Cl-(1:1:1:2) | ||
| C. | Ag+、NH4+、OH-、NO3-(1:3:3:1) | D. | K+、H+、I-、HCO3-(2:1:2:1) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com