


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
| A、Si→SiO2→H2SiO3→Na2SiO3 |
| B、Al→Al2O3→Al(OH)3→NaAlO2 |
| C、Na→NaOH→Na2CO3→NaHCO3 |
| D、Cu→CuO→Cu(OH)2→CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向含有少量CaCO3沉淀的水中通入CO2,沉淀溶解;再向溶液中加入Na2CO3溶液,又有CaCO3沉淀生成 |
| B、向Na2CO3溶液中逐滴加入含等物质的量HCl的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1:2 |
| C、等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,NaHCO3生成的CO2较多 |
| D、向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
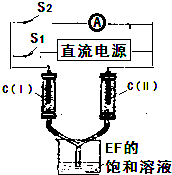
 A、B、C、D都是中学化学中的常见化合物,均由周期表前18号元素组成,D为红综色气体,甲、乙则是两种单质,以上单质和化合物之间有如图所示的反应关系(反应物和生成物均无省略),反应①②均是工业生产中的重要反应.
A、B、C、D都是中学化学中的常见化合物,均由周期表前18号元素组成,D为红综色气体,甲、乙则是两种单质,以上单质和化合物之间有如图所示的反应关系(反应物和生成物均无省略),反应①②均是工业生产中的重要反应.| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(C)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
| 容器编号 | n(甲) | n(C) | n (D) | v正与v逆的关系 |
| Ⅰ | 0.20 | 0.10 | 0.20 | v正=v逆 |
| Ⅱ | 0.20 | 0.40 | 1.00 | ②? |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有A、B、C、D、E、F、G七种前四周期元素,原子序数依次增大,其相关信息如表:
有A、B、C、D、E、F、G七种前四周期元素,原子序数依次增大,其相关信息如表:| 元素 | 元素的相关信息 |
| A | 存在多种核素,其中一种核素没有中子 |
| B | 核外电子排布式三个能级上的电子数相同 |
| C | 其第一电离能比同周期相邻元素的第一电离能都大 |
| D | 最外层电子数是内层电子数三倍的元素 |
| E | 单质或其化合物在火焰灼烧时,火焰呈黄色 |
| F | 位于第三周期ⅦA族 |
| G | 未成对电子数最多的副族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中 的能量变化 | ||
| SO2 | O2 | SO3 | ||
| ① | 2 | 1 | 0 | 放出热量a kJ |
| ② | 1 | 0.5 | 0 | 放出热量b kJ |
| ③ | 0 | 0 | 2 | 吸收热量c kJ |
| A、平衡时SO3气体的体积分数:③=①>② |
| B、a+c=196.4 |
| C、三个容器内反应的平衡常数:③=①=② |
| D、平衡时O2的浓度:①=③=2×② |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
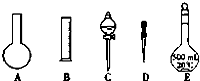 实验室需要0.1mol/L NaOH溶液450mL和0.6mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL和0.6mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤ | B、①②④⑤ |
| C、②④⑤ | D、③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com