
【题目】在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.01 mol的酸性混合溶液中加入0.01 mol铁粉,经搅拌后发生的变化应是 ( )
A. 铁溶解,析出0.01 mol Ag和0.005 mol Cu
B. 铁溶解,析出0.01 mol Ag并放出H2
C. 铁溶解,析出0.01 mol Ag,溶液中不再有Fe3+
D. 铁溶解,析出0.01 mol Ag,溶液中不再有Cu2+
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度,在实验室中进行如下实验,请完成下列填空:
(1) 配制100mL 0.10mol/L NaOH标准溶液。
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①滴定达到终点的现象是_______________________________________,此时锥形瓶内溶液的pH为________。
②根据上述数据,可计算出该盐酸的浓度约为____________________(保留两位有效数字)
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______。
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、称量前NaOH固体中混有Na2CO3固体
E、碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类或性质与应用均正确的是( )
A. Al2O3的熔点很高,可用于制作耐高温材料
B. Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒
C. 硅晶体是良好的半导体,可用于制造光导纤维
D. Al(OH)3是一种强碱,可以与酸反应,可用作医用的胃酸中和剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D分别代表四种不同的元素。A原子的最外层电子排布为ns1,B原子的价电子排布为ns2np2,C原子的最外层电子数是其电子层数的3倍,D原子的L电子层的p轨道有3个电子。
(1)C原子的电子排布式为__________________,若A原子的最外层电子排布为1s1,则按原子轨道的重叠方式判断,A与C形成的化合物中的共价键类型属于______键。
(2)上述化合物A2C的熔沸点高于化合物DA3的熔沸点,其主要原因可能是____________;
(3)当n=2时,B与C形成的晶体属于 _______晶体,B与C形成的最高价化合物的结构式为_________________ 。
(4)当n=3时,B与C形成的晶体属于_______晶体,其晶体结构如下图所示。该晶体中最小的环由______个微粒构成,一个晶胞中含有______个B微粒,______个C微粒。
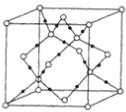
(5)若A原子的最外层电子排布为4s1,B原子的价电子排布为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序为 _______________________ (用元素符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下发生反应:2X(g)![]() Y(g)+3Z(g) △H=akJ·mol-1(a>0)下列说法正确的是
Y(g)+3Z(g) △H=akJ·mol-1(a>0)下列说法正确的是
A. 增大X的浓度,正反应速率增大,逆反应速率减小
B. 将0.2molX充入反应器中,充分反应后,生成的Z的物质的量可能为0.09mol
C. 达到化学平衡状态时,正、逆反应的速率都为0
D. 达到化学平衡状态时,共吸收a kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是( )
A. MnO2与浓盐酸反应制Cl2:MnO2+4HCl![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
B. 明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+
C. Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑
D. Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com